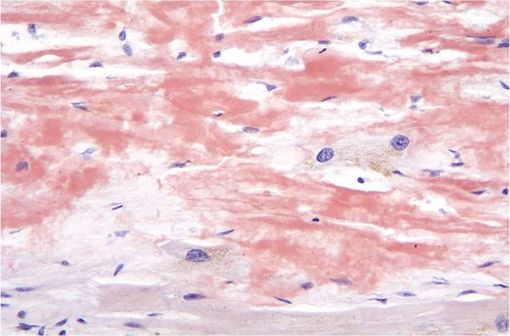
Photomicrographie montrant des dépôts amyloïdes (structures réhaussées de rouge) dans le cœur (amylose cardiaque). Coloration au rouge congo (illustration @Nephron sur Wikimedia).
Résumé :
VYNDAQEL 61 mg capsule molle (tafamidis micronisé) est indiquée dans la forme cardiaque de l'amylose à transthyrétine, c'est-à-dire chez les patients adultes présentant une cardiomyopathie (ATTR-CM).
Il s'agit d'un nouveau dosage à 61 mg de tafamidis micronisé, qui s'ajoute à VYNDAQEL 20 mg capsule molle, à base de tafamidis méglumine, déjà disponible, mais dans une autre indication. VYNDAQEL 20 mg est en effet à visée symptomatique pour ralentir le déficit neurologique périphérique de l'amylose à transthyrétine.
Le tafamidis micronisé et le tafamidis méglumine ne sont pas interchangeables en mg.
Suite à l'évaluation médico-économique réalisée par la Commission de la Transparence (CT), VYNDAQEL 61 mg capsule molle a obtenu un service médical rendu (SMR) important et une amélioration du service médical rendu importante (ASMR II).
Pour traiter la forme cardiaque de l'amylose à transthyrétine, la posologie est de 61 mg de tafamidis par jour (1 capsule molle de VYNDAQEL 61 mg par jour). Le traitement doit être initié le plus tôt possible pour limiter la progression de la maladie.
VYNDAQEL 61 mg capsule molle est agréé aux collectivités et remboursable à 65 %, avec une base de remboursement fixée à 7 261,02 euros TTC (1 boîte de 30).
VYNDAQEL 61 mg capsule molle (tafamidis micronisé) est indiquée dans la forme cardiaque de l'amylose à transthyrétine, c'est-à-dire chez les patients adultes présentant une cardiomyopathie (ATTR-CM).
Il s'agit d'un nouveau dosage à 61 mg de tafamidis micronisé, qui s'ajoute à VYNDAQEL 20 mg capsule molle, à base de tafamidis méglumine, déjà disponible, mais dans une autre indication. VYNDAQEL 20 mg est en effet à visée symptomatique pour ralentir le déficit neurologique périphérique de l'amylose à transthyrétine.
Le tafamidis micronisé et le tafamidis méglumine ne sont pas interchangeables en mg.
Suite à l'évaluation médico-économique réalisée par la Commission de la Transparence (CT), VYNDAQEL 61 mg capsule molle a obtenu un service médical rendu (SMR) important et une amélioration du service médical rendu importante (ASMR II).
Pour traiter la forme cardiaque de l'amylose à transthyrétine, la posologie est de 61 mg de tafamidis par jour (1 capsule molle de VYNDAQEL 61 mg par jour). Le traitement doit être initié le plus tôt possible pour limiter la progression de la maladie.
VYNDAQEL 61 mg capsule molle est agréé aux collectivités et remboursable à 65 %, avec une base de remboursement fixée à 7 261,02 euros TTC (1 boîte de 30).
La gamme VYNDAQEL capsule molle compte un nouveau dosage à 61mg de tafamidis micronisé, indiquée dans l'amylose à transthyrétine de type sauvage ou héréditaire chez les patients adultes présentant une cardiomyopathie (ATTR-CM) [cf. Encadré 1].
Encadré 1 - Amylose à transthyrétine : forme cardiaque (source HAS)
| L'amylose à transthyrétine (ATTR) est une maladie liée à une anomalie de la transthyrétine (TTR), protéine impliquée dans le transport de la thyroxine. L'anomalie peut être génétique, liée à une mutation sur le gène de la transthyrétine, c'est la forme dite héréditaire, à transmission autosomique dominante. Elle peut également être due aux dépôts d'une forme anormale de transthyrétine dite sénile, c'est la forme sauvage. Une amylose à transthyrétine avec cardiomyopathie (ATTR-CM) peut être suspectée chez les patients présentant une insuffisance cardiaque à fraction d'éjection préservée, le plus souvent en présence d'une hypertrophie pariétale du ventricule gauche. Les atteintes cardiovasculaires décrites dans la maladie sont notamment :
|
VYNDAQEL est déjà disponible sous un autre dosage, à 20 mg de tafamidis méglumine (et non tafamidis micronisé), dans une indication différente de celle du dosage à 61 mg. Il est en effet indiqué à visée symptomatique pour ralentir le déficit neurologique périphérique dans le cadre d'une ATTR.
Le traitement par VYNDAQEL doit être initié par un médecin expérimenté dans la prise en charge de patients ayant une ATTR-CM.
VYNDAQEL 61 mg capsule molle fait l'objet d'une surveillance supplémentaire qui permettra l'identification rapide de nouvelles informations relatives à la sécurité. Les professionnels de la santé déclarent tout effet indésirable suspecté.
Un besoin thérapeutique non couvert jusqu'à présent
VYNDAQEL 61 mg est le premier médicament disposant d'une autorisation de mise sur le marché (AMM) dans le traitement de l'ATTR-CM. Il s'agit d'une maladie rare dont la population cible en France est estimée à 5 000 patients selon la Haute Autorité de Santé.
L'autre dosage de VYNDAQEL, à 20 mg de tafamidis méglumine, bénéficie pour sa part, en plus de son indication d'AMM dans la forme neurologique de l'ATTR, d'une recommandation temporaire d'utilisation (RTU) depuis 2018 dans le traitement de l'amylose cardiaque héréditaire ou sauvage à transthyrétine chez les patients adultes atteints d'insuffisance cardiaque restrictive de classe NYHA I, II ou III (ATTR-CM). Les données d'utilisation de ce médicament sous ce statut ont été prises en compte dans l'avis de la Commission de la Transparence (CT) sur ce médicament.
Une supériorité démontrée versus placebo en termes de mortalité et d'hospitalisations
L'efficacité et la tolérance du tafamidis dans l'ATTR-CM ont été évaluées dans l'étude de supériorité B3461028 (1) ou ATTR-ACT (Tafamidis Treatment for Patients with Transthyretin Amyloid Cardiomyopathy).
Cette étude de phase III multicentrique, contrôlée, randomisée, en double aveugle, en groupe parallèles, comparative versus placebo, a évalué l'efficacité d'une dose journalière de 20 mg (ne correspondant pas à celle de l'AMM) ou 80 mg de tafamidis méglumine sur la mortalité toutes causes confondues et la fréquence d'hospitalisation pour cause cardiovasculaire (critère de jugement principal composite hiérarchisé) :
- mortalité toutes causes confondues à 30 mois ;
- fréquence d'hospitalisation pour cause cardiovasculaire sur 30 mois définie comme le nombre de fois qu'un sujet a été hospitalisé (c'est-à-dire admis dans un hôpital) pour une morbidité liée à une maladie cardiovasculaire.
Selon les résultats de cette étude, la supériorité de VYNDAQEL à été démontrée par rapport au placebo :
- le nombre de patients décédés a été de 23 (26,1 %) dans le groupe tafamidis 20 mg (n = 88), de 49 (27,8 %) dans le groupe tafamidis 80 mg (n = 176) et de 72 (40,7 %) dans le groupe placebo (n = 177), avec un hazard ratio de 0,70 (IC95 % = [0,51 ; 0,96], p = 0,0259), statistiquement significatif en faveur du groupe tafamidis (calculé sur la base des 2 groupes tafamidis combinés) ;
- la fréquence d'hospitalisation pour cause cardiovasculaire a été de 0,48 pour le groupe tafamidis versus 0,70 pour le groupe placebo, avec un risque relatif de 0,68 (IC95 % = [0,56 ; 0,81]) p < 0,0001), soit un résultat statistiquement significatif en faveur du groupe tafamidis.
VYNDAQEL a également été supérieur au placebo sur 2 critères de jugement secondaires hiérarchisés :
- la variation par rapport à l'inclusion de la distance parcourue au test de marche de 6 minutes (6MWT) au 30e mois,
- et la variation par rapport à l'inclusion du score global au questionnaire de qualité de vie sur la cardiomyopathie de Kansas City (KCCQ-OS) au 30e mois.
Enfin, la CT considère que le profil de tolérance du tafamidis est satisfaisant car les événements indésirables cardiaques observé dans l'étude clinique "sont à mettre en perspective avec les symptômes et la gravité de la pathologie sous-jacente". Par ailleurs, elle indique que "le recul d'utilisation du tafamidis sur plusieurs années dans l'ATTR pour la forme polyneuropathie a été considéré comme rassurant".
Un SMR important et une ASMR de niveau II
À l'issue de l'évaluation médico-économique, la CT a émis un avis (avis du 23 septembre 2020) dans lequel elle attribue à VYNDAQEL 61 mg, dans le traitement de l'ATTR-CM :
- un service médical rendu (SMR) important ;
- une amélioration du service médical rendu importante (ASMR de niveau II).
Dans la stratégie thérapeutique, VYNDAQEL (tafamidis) est un traitement de 1re intention de l'amylose à transthyrétine avec cardiomyopathie, d'autant plus qu'il est le seul à disposer de cette indication.
Cas de patients ATTR avec atteinte cardiaque et neurologique
Pour les patients ayant une ATTR avec à la fois une atteinte cardiaque et une atteinte neurologique, la CT ne se prononce pas, faute de données, sur la stratégie d'utilisation conjointe ou séquentielle des différents traitements existants :
- ONPATTRO (patisiran) (cf. notre article du 4 janvier 2021),
- TEGSEDI (inotersen) (cf. notre article du 20 janvier 2021),
- VYNDAQEL 20 mg (tafamidis méglumine),
- VYNDAQEL 61 mg (tafamidis micronisé).
VYNDAQEL 61 mg en pratique
Une initiation précoce du traitement par VYNDAQEL dans l'évolution de la maladie permet d'apporter des bénéfices cliniques sur la progression de la maladie. Lorsque les lésions cardiaques liées à l'amylose sont plus avancées, comme dans la classe III de la NYHA, la décision de débuter ou de poursuivre le traitement doit être prise à la discrétion d'un médecin compétent dans la prise en charge des patients atteints d'amylose ou de cardiomyopathie.
Schéma posologique : 1 capsule molle de 61 mg par jour
La posologie recommandée est de 61 mg de tafamidis (soit 1 capsule molle de VYNDAQEL 61 mg), administrés par voie orale en une prise journalière.
VYNDAQEL 61 mg (tafamidis) équivaut à 80 mg de tafamidis méglumine (4 capsules molles de VYNDAQEL 20 mg). Cependant, le tafamidis et le tafamidis méglumine ne sont pas interchangeables en mg.
Contraception et tafamidis
Les femmes en âge de procréer doivent utiliser une contraception efficace lorsqu'elles sont traitées par tafamidis et doivent continuer à utiliser une contraception efficace pendant 1 mois après l'arrêt du traitement par tafamidis
Identité administrative
- Liste I
- Boîte de 30, CIP 3400930202074
- Remboursable à 65 % (Journal officiel du 26 mai 2021, texte 11)
- Prix public TTC = 7 261,02 euros
- Agrément aux collectivités (Journal officiel du 26 mai 2021 - texte 12)
- Laboratoire Pfizer
Pour aller plus loin
Avis de la Commission de la Transparence - VYNDAQEL 61 mg (HAS, 23 septembre 2020)
L'étude pivot
(1) Maurer MS, Schwartz JH et al. Tafamidis treatment for patients with transthyretin amyloid cardiomyopathy. N Engl J Med. 2018 ; 379 : 1007-16
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 6 minutes
6 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.