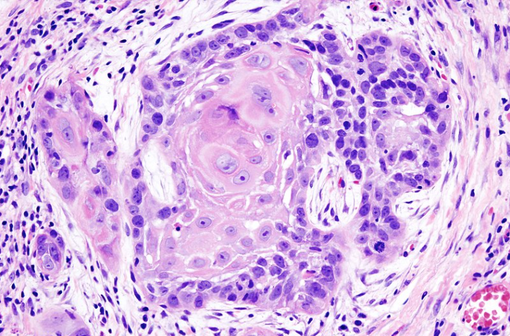
Carcinome épidermoïde invasif bien différencié (illustration @Wikimedia).
L'arsenal thérapeutique du carcinome épidermoïde cutané compte une nouvelle spécialité, LIBTAYO 350 mg solution à diluer pour perfusion IV (intraveineuse), réservée à l'usage hospitalier.
LIBTAYO est indiqué en monothérapie dans le traitement de patients adultes atteints d'un carcinome épidermoïde cutané métastatique ou localement avancé (CECm ou CECla) qui ne sont pas candidats à une chirurgie curative ni à une radiothérapie curative (cf. VIDAL Reco "Mélanome").
LIBTAYO fait l'objet d'une surveillance supplémentaire qui permettra l'identification rapide de nouvelles informations relatives à la sécurité. Les professionnels de santé déclarent tout effet indésirable suspecté.
Un nouvel anticorps monoclonal
Le principe actif de LIBTAYO est un nouvel anticorps monoclonal, le cémiplimab.
Il s'agit d'un anticorps monoclonal entièrement humain, de type G4 (IgG4). En se liant au récepteur de mort cellulaire programmé-1 (PD-1) sur les cellules T, le cémiplimab permet d'empêcher la neutralisation de ces cellules immunitaires par le PD-L1 et PD-L2 produits par les cellules tumorales.
En France, le cémiplimab a bénéficié d'une ATU (autorisation temporaire d'utilisation) nominative, puis d'une ATU de cohorte entre avril 2019 et octobre 2019.
Il a obtenu une AMM (autorisation de mise sur le marché) conditionnelle européenne en 2020 sous le nom LIBTAYO, sur la base des résultats d'une étude de phase II non comparative.
De nouvelles études sont attendues pour confirmer cette AMM :
- étude visant à confirmer l'efficacité et la sécurité du cémiplimab pour le traitement des patients atteints d'un carcinome épidermoïde cutané métastatique ou localement avancé dans le cadre prévu par l'AMM,
- étude de comparaison cémiplimab versus placebo (étude randomisée, en double aveugle évaluant en adjuvant cémiplimab versus placebo après radiothérapie chez des patients présentant un cancer épidermoïde cutané à haut risque).
Évaluation médico-économique : SMR faible à l'issue de la première évaluation
La demande de prise en charge de LIBTAYO a été examinée par la Commission de Transparence (CT) en mars 2020.
Dans son avis du 18 mars 2020, la CT a attribué un SMR (service médical rendu) faible à LIBTAYO, dans l'indication de l'AMM.
Cet avis repose sur les données d'efficacité et de tolérance du cémiplimab (LIBTAYO) obtenues dans l'étude de phase II non comparative (étude R2810-ONC-1540), selon 2 schémas posologiques (3 mg/kg toutes les 2 semaines pendant 96 semaines, ou 350 mg toutes les 3 semaines pendant 54 semaines). Cette étude a été réalisée sur 3 cohortes de patients atteints d'un carcinome épidermoïde cutané, inéligibles à la chirurgie et à la radiothérapie :
- Cohorte 1 : métastatique traitée par 3 mg/kg toutes les deux semaines (N = 59) ;
- Cohorte 2 : localement avancé traitée par 3 mg/kg toutes les deux semaines (N = 78) ;
- Cohorte 3 : métastatique traitée par 350 mg toutes les 3 semaines (N = 56)
Le pourcentage de réponse objective (ORR) évaluée par un comité mixte d'experts indépendants pour chaque cohorte (critère de jugement principal) a été de 49,2 % et 39,3 % dans les cohortes "métastatiques" 1 et 3 respectivement, et de 43,6 % dans la cohorte 2 "localement avancé".
La survie sans progression médiane a été de 18,4 mois (IC95 % [7,3 ; NE]) et de 10,4 mois (IC95 % [3,6 ; NE]) pour les patients "métastatiques" des cohortes métastatiques 1 et 3 et n'était pas encore atteinte dans la cohorte "localement avancé".
En termes de tolérance, les données sont limitées. Les principales toxicités relevées ayant été cependant d'ordre immunologique et respiratoire (principalement la pneumopathie inflammatoire).
Une place dans la stratégie thérapeutique qui reste à préciser
Faute de données comparant LIBTAYO avec les alternatives thérapeutiques actuellement disponibles et dans l'attente de nouvelles données d'efficacité et de sécurité, la CT considère que LIBTAYO est :
- une option thérapeutique de 1re ligne de traitement carcinome épidermoïde cutané ne relevant pas de la chirurgie ou de la radiothérapie,
- mais sa place dans la stratégie thérapeutique reste à préciser.
La population cible est estimée à environ 1 000 patients par an (cf. Encadré 1).
Encadré 1 - Prise en charge actuelle des carcinomes épidermoïdes cutanés chez les patients non éligibles à la radiothérapie et à la chirurgie (extrait de l'avis de la HAS)
| La plupart des carcinomes épidermoïdes cutanés sont de bon pronostic car facilement traités par chirurgie, voire radiothérapie. Cependant, dans de très rares cas, ces lésions progressent vers des formes localement avancées qui ne permettent plus de recourir à la chirurgie ni à la radiothérapie curative (CECla) et vers des formes avec métastases intra-lymphatiques, ganglionnaires puis à distance (CECm). À ce jour, les stades avancés ne relevant pas de la chirurgie ou de la radiothérapie sont traités, pour les patients éligibles, par chimiothérapie systémique dont les résultats sont faibles, ou par des thérapies ciblées anti EGFR utilisées hors AMM (géfitinib, cétuximab, panitumumab). |
LIBTAYO en pratique : solution à diluer avant administration
Le traitement doit être prescrit et surveillé par des médecins qualifiés et expérimentés dans le traitement des cancers.
LIBTAYO se présente en flacon à usage unique, contenant 7 mL de solution (350 mg de cémiplimab).
Le flacon doit être conservé au réfrigérateur (entre 2 et 8 °C), à l'abri de la lumière.
Avant l'administration, la solution de LIBTAYO doit être diluée dans une poche de perfusion intraveineuse (chlorure de sodium 0,9 % ou glucose 5 %)
Administration en perfusion IV toutes les 3 semaines
La dose recommandée est de 350 mg de cémiplimab (dose contenue dans 1 flacon), administrée toutes les 3 semaines par perfusion IV (intraveineuse) de 30 minutes. Il est recommandé d'utiliser une tubulure pour voie IV intégrant un filtre ou avec un filtre stérile, apyrogène, à faible fixation protéique, en ligne ou additionnel (diamètre pore 0,2 à 5 microns). Aucun autre médicament ne doit être passé dans la même tubulure.
Le traitement pourra être poursuivi jusqu'à la progression de la maladie ou la survenue d'une toxicité inacceptable.
Gestion des événements indésirables
LIBTAYO expose à des événements indésirables (EI) divers :
- EI d'origine immunologique, pouvant atteindre divers organes : pneumopathie inflammatoire, colite, hépatite, hypothyroïdie, hyperthyroïdie, hypophysite, insuffisance surrénalienne, diabète de type 1, cutanés (syndrome de Stevens-Johnson), néphrite avec insuffisance rénale, etc.,
- réactions liées à la perfusion.
En cas d'événement indésirable, aucune réduction de dose n'est recommandée.
En revanche, les actions suivantes peuvent être mises en place, selon la sévérité de l'événement indésirable :
- reporter l'administration ou ralentir le débit de la perfusion,
- interrompre le traitement,
- ou l'arrêter définitivement.
Selon les situations, un traitement symptomatique est également recommandé.
NB. Des effets indésirables d'origine immunologique peuvent apparaître après l'arrêt du cémiplimab.
Dispositif d'information pour les patients
Pour accompagner les prescripteurs et informer les patients sur les EI associés à LIBTAYO, des documents éducationnels ont été élaborés :
- un guide d'information,
- une carte d'alerte patient.
Ces documents destinés aux patients sont prévus dans le plan de gestion des risques de ce médicament. Ils précisent la conduite à tenir en présence d'un symptôme évoquant un EI d'origine immunologique et de réactions à la perfusion.
La Carte d'Alerte Patient (cf. Encadré 2) doit être remise à chaque patient, par le médecin prescripteur. Le patient doit conserver ce document avec lui.
Encadré 2 - Éléments-clés figurant dans la carte d'alerte patient
|
Identité administrative
- Liste I
- Réservé à l'usage hospitalier
- Prescription réservée aux spécialistes en oncologie ou aux médecins compétents en cancérologie
- Surveillance particulière pendant le traitement
- Flacon de 350 mg dans une solution de 7 mL, à usage unique, CIP 3400955067283
- Agrément aux collectivités (Journal officiel du 22 janvier 2021 - texte 29)
- Laboratoire Sanofi-aventis France
Pour aller plus loin
Avis de la Commission de la Transparence - LIBTAYO (HAS, 18 mars 2020)
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 6 minutes
6 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.