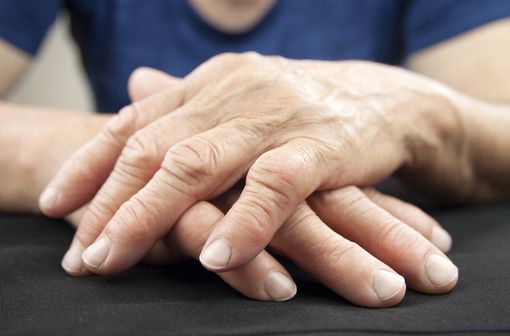
La polyarthrite rhumatoïde commence le plus souvent par un enraidissement douloureux de plusieurs articulations, généralement les poignets, les mains et les doigts (illustration).
Une nouvelle présentation de l'inhibiteur des Janus kinases à base de tofacitinib est mise à disposition en France : XELJANZ 11 mg comprimé à libération prolongée (LP), en complément des présentations existantes XELJANZ 5 mg et 10 mg comprimés pelliculés.
XELJANZ 11 mg LP est indiqué uniquement en rhumatologie (cf. Encadrés 1 et 2), dans le traitement de la polyarthrite rhumatoïde (cf. VIDAL Reco "Polyarthrite rhumatoïde") et plus précisément :
- en association avec du méthotrexate (MTX), dans le traitement de la polyarthrite rhumatoïde (PR) active, modérée à sévère chez les patients adultes ayant présenté une réponse inadéquate ou une intolérance à un ou plusieurs traitements de fond antirhumatismaux (DMARDs : Disease-Modifying Antirheumatic Drugs). Le tofacitinib peut être administré en monothérapie en cas d'intolérance au MTX ou lorsque le traitement avec le MTX est inadapté.
Encadré 1 - XELJANZ : comparaison des indications remboursables selon les présentations
| XELJANZ 5 mg comprimé | XELJANZ 10 mg comprimé | XELJANZ 11 mg comprimé LP | |
| Polyarthrite rhumatoïde | x | - | x |
| Rhumatisme psoriasique | x | - | - |
| Rectocolite hémorragique | x | x | - |
Encadré 2 - Indications thérapeutiques du tofacitinib
|
XELJANZ 11 mg comprimé LP fait l'objet d'une surveillance supplémentaire qui permettra l'identification rapide de nouvelles informations relatives à la sécurité. Les professionnels de santé déclarent tout effet indésirable suspecté.
Nouveau dosage et forme à libération prolongée
XELJANZ 11 mg comprimé LP est la présentation la plus dosée de la gamme en tofacitinib.
Il se distingue également des autres présentations de la gamme par sa formulation à libération prolongée, caractérisée par des concentrations plasmatiques maximales atteintes en 4 heures et une demi-vie d'environ 6 heures. Les concentrations à l'état d'équilibre sont atteintes dans les 48 heures, avec une accumulation négligeable après une administration quotidienne. À titre de comparaison, les concentrations plasmatiques maximales de XELJANZ 5 mg sont atteintes en 0,5 à 1 heure et l'élimination est rapide (demi-vie d'environ 3 heures).
L'équivalence pharmacocinétique (AUC et Cmax) entre le tofacitinib 11 mg comprimé LP 1 fois par jour et le tofacitinib 5 mg comprimé pelliculé 2 fois par jour a été démontrée.
En tant que complément de gamme et du fait de son équivalence pharmacocinétique avec XELJANZ 5 mg, un service médical rendu (SMR) important a été attribué à XELJANZ LP 11 mg dans son indication. Toutes les études d'efficacité et de sécurité du tofacitinib ont été menées avec les dosages à 5 mg ou 10 mg en comprimé.
XELJANZ 11 mg LP en pratique
La dose recommandée de XELJANZ 11 mg est de 1 comprimé LP administré 1 fois par jour. Cette posologie ne doit pas être dépassée.
Passage de la forme à libération immédiate à la forme LP
Du fait de leur équivalence pharmacocinétique, il est possible de passer de la forme à libération immédiate XELJANZ 5 mg à la forme à libération prolongée XELJANZ LP 11 mg, et inversement, selon les modalités suivantes :
- les patients traités avec tofacitinib 5 mg comprimé pelliculé 2 fois par jour peuvent passer au tofacitinib 11 mg comprimé LP 1 fois par jour, le jour suivant l'administration de la dernière dose de tofacitinib 5 mg comprimé pelliculé ;
- les patients traités avec tofacitinib 11 mg comprimé LP 1 fois par jour peuvent passer au tofacitinib 5 mg comprimé pelliculé 2 fois par jour, le jour suivant l'administration de la dernière dose de tofacitinib 11 mg comprimé LP.
Éléments à prendre en compte avant d'initier le traitement par XELJANZ
Il est recommandé de ne pas initier le traitement chez les patients présentant :
- une numération absolue des lymphocytes (NAL) inférieure à 750 cellules/mm3 ;
- une numération absolue des neutrophiles (NAN) inférieure à 1000 cellules/mm3 ;
- un taux d'hémoglobine inférieur à 9 g/dL.
Ajustement de la dose ou arrêt du traitement
Des ajustements posologiques sont nécessaires dans les situations suivantes :
- insuffisance hépatique,
- insuffisance rénale,
- administration concomitante de médicaments inhibiteurs puissants du cytochrome P450 3A4 (kétoconazole par exemple) et médicaments entraînant une inhibition modérée du CYP3A4 ainsi qu'une inhibition puissante du CYP2C19 (par exemple le fluconazole).
Une surveillance de la numération formule sanguine est nécessaire pendant le traitement par XELJANZ. Le traitement doit être suspendu ou arrêté en fonction des résultats portant sur :
- la NAL,
- la NAN,
- le taux d'hémoglobine.
Attention au risque de thrombose veineuse et d'infection
En février 2020 (cf. notre article du 10 février 2020), le tofacitinib a fait l'objet d'une réévaluation européenne, à l'issue de laquelle les recommandations suivantes ont été émises :
Ces risques et recommandations sont précisés dans la rubrique "Mises en garde et précautions d'emploi" de la monographie VIDAL.
- le tofacitinib est associé :
- à une augmentation du risque de MTEV (maladie thromboembolique veineuse) grave, comprenant des embolies pulmonaires (EP) et des thromboses veineuses profondes (TVP),
- à une augmentation des infections graves et infections létales, en particulier chez les plus de 65 ans ;
- une relation dose-dépendante entre le tofacitinib et les effets indésirables cardiovasculaires est rapportée ;
- le tofacitinib doit être utilisé avec prudence chez les patients présentant des facteurs de risque connus de MTEV, quelle que soit l'indication (pour les dosages à 5 et 10 mg : polyarthrite rhumatoïde, rhumatisme psoriasique, rectocolite hémorragique) et la posologie ;
- le tofacitinib ne doit pas être utilisé à la dose de 10 mg 2 fois par jour chez les patients atteints de rectocolite hémorragique présentant des facteurs de risque de MTEV, sauf en l'absence d'alternative thérapeutique ;
- le tofacitinib ne doit pas être envisagé chez les patients de plus de 65 ans en raison du risque d'infection, sauf en l'absence d'alternative appropriée.
Ces risques et recommandations sont précisés dans la rubrique "Mises en garde et précautions d'emploi" de la monographie VIDAL.
- Liste I
- Prescription initiale hospitalière annuelle
- Prescription initiale et renouvellement réservés aux spécialistes en rhumatologie
- Boîte de 28 comprimés, CIP 3400930199893
- Remboursable à 65 % selon la procédure des médicaments d'exception (Fiche d'information thérapeutique publiée au Journal officiel du 22 décembre 2020 - texte 32) [cf. Encadré 3]
- Prix public TTC = 703,01 euros
- Agrément aux collectivités (Journal officiel du 22 décembre 2020 - texte 33)
- Laboratoire Pfizer
Encadré 3 - Périmètre de remboursement de XELJANZ LP 11 mg
| Traitement de la polyarthrite rhumatoïde (PR) active, modérée à sévère, en association au méthotrexate (MTX), chez les patients adultes ayant présenté une réponse inadéquate ou une intolérance à un ou plusieurs traitements de fond antirhumatismaux (DMARDs : Disease Modifying Antirheumatic Drugs). |
Pour aller plus loin
Avis de la Commission de la Transparence - XELJANZ LP 11 mg (HAS, 22 avril 2020)
Sur VIDAL.fr
XELJANZ (TOFACITINIB) : UTILISATION PRUDENTE VOIRE NON RECOMMANDÉE CHEZ LES PATIENTS À RISQUE ÉLEVÉ DE THROMBOSE (10 février 2020)
XELJANZ (TOFACITINIB) : RESTRICTION D'UTILISATION EN CAS DE RISQUE ÉLEVÉ D'EMBOLIE PULMONAIRE (11 juin 2019)
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 6 minutes
6 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.