
La kératoconjonctivite vernale (KCV) est une forme rare d'allergie oculaire survenant principalement chez l'enfant (illustration).
La kératoconjonctivite vernale sévère de l'enfant à partir de 4 ans et de l'adolescent (cf. Encadré 1) dispose désormais d'un médicament spécifique à base de ciclosporine : VERKAZIA 1 mg/mL collyre en émulsion.
Encadré 1 - La kératoconjonctivite vernale : une allergie pédiatrique rare
| La kératoconjonctivite vernale (KCV) est une forme rare d'allergie oculaire survenant principalement chez l'enfant. Elle se traduit par une inflammation chronique de la surface oculaire (conjonctivite et atteinte de la cornée) et des exacerbations saisonnières au printemps et en été. Dans 8 cas sur 10, la KCV survient avant 10 ans. En France, la prévalence de KCV en France est estimée entre 0,7 et 3,3 pour 10 000 habitants, avec une prédominance masculine. |
VERKAZIA est conditionné en unidose, sans conservateur.
D'aspect blanc laiteux, l'émulsion est formulée à base de triglycérides à chaîne moyenne et de chlorure de cétalkonium (CKC), utilisé ici comme surfactant cationique. Les propriétés lipophiles du CKC permettent une meilleure stabilisation des gouttelettes huileuses contenant la ciclosporine.
Première spécialité à base de ciclosporine en collyre indiquée dans la KCV
VERKAZIA est la première spécialité de ciclosporine en collyre disposant d'une AMM (autorisation de mise sur le marché) pour traiter les KCV sévères chez les enfants et les adolescents.
Jusqu'à présent, en l'absence de médicaments, les ophtalmologistes français utilisaient des préparations hospitalières ophtalmiques à base de ciclosporine extraite des comprimés de ciclosporine (NEORAL, SANDIMUN) et non standardisées. Ces préparations ont des concentrations comprises entre 0,05 % et 2 % et sont présentées en flacon multidose. En outre, une utilisation hors AMM des collyres de ciclosporine IKERVIS (spécialité hospitalière) et RESTASIS (ATU nominative) est signalée.
Dans son avis du 22 janvier 2020, la HAS (Haute Autorité de Santé) souligne que les données cliniques disponibles pour ces préparations sont limitées et anciennes : "Il persiste donc un besoin médical à disposer de traitements de fond ayant une AMM validée, comme VERKAZIA, dans le traitement de la KCV sévère".
SMR important, ASMR IV
Dans cet avis, la Commission de la Transparence de la HAS a évalué l'efficacité de VERKAZIA sur la base de l'étude de phase III de supériorité versus véhicule, randomisée, en double aveugle, en groupes parallèles, multicentrique, VEKTIS III (n = 168, âge moyen 9,1 ans), ayant comparé l'émulsion de ciclosporine 1 mg/mL (2 posologies étudiées : 1 goutte 4 fois ou 2 fois par jour) versus véhicule (émulsion). Cette étude comportait une période de traitement de 4 mois (période I) et une période de suivi de 8 mois (période II) au cours de laquelle les patients du groupe ciclosporine ont pu poursuivre leur traitement et les patients du groupe véhicule ont été randomisés en deux groupes pour recevoir la ciclosporine selon l'un ou l'autre des 2 schémas posologiques.
Le critère de jugement principal était la variation sur 4 mois du score de coloration cornéenne à la fluorescéine (CFS ou Corneal Fluorescein Staining évalué à l'aide de l'échelle modifiée d'Oxford et défini comme la moyenne des 4 scores mesurés à chaque visite mensuelle), ajusté en fonction de pénalités :
- nécessité d'un traitement de secours (dexaméthasone à usage local),
- occurrence d'ulcération de la cornée.
L'efficacité était déterminée sur l'œil le plus sévèrement atteint (score CFS le plus élevé). Si les deux yeux avaient le même score, l'œil droit était choisi.
Selon les résultats de cette étude, la variation moyenne du score CFS ajusté sur les pénalités au cours des 4 premiers mois de traitement a été plus élevée dans les groupes ciclosporine 1 mg/mL que dans le groupe véhicule (cf. Tableau I).
Tableau I - Réduction moyenne (en valeur absolue) du score CFS ajusté sur les pénalités au cours des 4 mois de traitement par rapport à l'inclusion (FAS avec imputation des données manquantes)
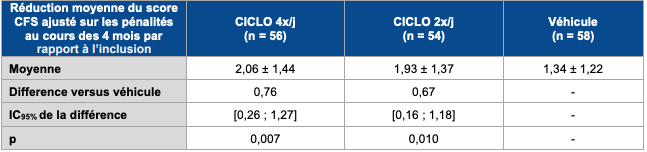
La Commission précise qu'"à titre indicatif, l'analyse de la contribution des 3 composantes du critère de jugement principal composite a montré que pour la dose ciclosporine 1 mg/mL 4 x/j, le score CFS représentait 70,3 % de l'effet, le nombre moyen d'utilisation de traitements de secours par mois 29,6 % et le nombre moyen d'occurrence d'ulcère par mois 0,1 %".
En termes de tolérance, le pourcentage de patients ayant eu au moins un effet indésirable (EI) considéré comme lié au traitement au cours de la période totale de l'étude a été de 20,0 % (n = 10) chez les patients traités par ciclosporine 4x/j depuis le début de l'étude. Il s'agissait principalement d'EI locaux légers à modérés et transitoires, associés à l'instillation, tels que douleur et prurit oculaires.
Au terme de son évaluation, la Commission de la Transparence a attribué à VERKAZIA :
- un SMR (service médical rendu) important,
- une amélioration du SMR mineure (ASMR IV).
Un traitement de seconde intention dans la stratégie thérapeutique
La stratégie thérapeutique pour la KCV actuellement recommandée (Société française d'ophtalmologie - 2015) repose sur :
- un rinçage oculaire par du sérum physiologique,
- des collyres anti-allergiques et des corticoïdes locaux prescrits à court terme en raison du risque de glaucome et de cataracte.
En conclusion de son avis, la Commission considère donc que la place de VERKAZIA dans la stratégie thérapeutique est celle d'un traitement de seconde intention dans la KCV sévère de l'enfant et l'adolescent, en échec des collyres antiallergiques et corticodépendante.
VERKAZIA en pratique
Le traitement par VERKAZIA doit être instauré par un ophtalmologiste ou un professionnel de santé compétent en ophtalmologie.
- Une posologie à adapter à la saison et aux symptômes
Après la fin de la saison, si les signes et symptômes de la KCV persistent, le traitement peut être maintenu à la dose recommandée ou à une dose réduite à 1 goutte 2 fois par jour dès lors que les signes et symptômes sont contrôlés de façon satisfaisante.
Le traitement doit être arrêté après la disparition des signes et symptômes, et réinstauré si ceux-ci réapparaissent.
- Quelques consignes à respecter lors de l'instillation
- se laver les mains avant d'utiliser le collyre,
- agiter doucement le récipient unidose avant l'emploi,
- jeter l'unidose après l'utilisation (chaque unidose est à usage unique),
- pratiquer une occlusion naso-lacrymale et fermer les paupières pendant 2 minutes après administration afin de réduire le passage systémique.
- VERKAZIA et les autres collyres
- respecter un intervalle d'au moins 15 minutes entre chaque administration ;
- instiller VERKAZIA en dernier.
Identité administrative
- Liste I
- Prescription réservée aux spécialistes en ophtalmologie
- Boîte de 120 unidoses de 0,3 mL, CIP 3400930172032
- Remboursable à 65 % (Journal officiel du 10 octobre 2020, texte 24)
- Prix public TTC = 363,09 euros
- Agrément aux collectivités (Journal officiel du 10 octobre 2020, texte 25)
- Laboratoire Santen
Pour aller plus loin
Avis de la Commission de la Transparence - VERKAZIA (HAS, 22 janvier 2020)
Cet article d'actualité rédigé par un auteur scientifique reflète l'état des connaissances sur le sujet traité à la date de sa publication. Il ne s'agit pas d'une page encyclopédique régulièrement remise à jour. L'évolution ultérieure des connaissances scientifiques peut le rendre en tout ou partie caduc.
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire


Les commentaires sont momentanément désactivés
La publication de commentaires est momentanément indisponible.