
OROBUPRE lyophilisat oral est indiqué dans le traitement substitutif de la pharmacodépendance aux opioïdes (illustration).
Nouveau traitement substitutif de la pharmacodépendance aux opioïdes
OROBUPRÉ lyophilisat oral est une nouvelle spécialité de buprénorphine, indiquée dans le traitement substitutif de la pharmacodépendance aux opioïdes, dans le cadre d'une prise en charge médicale, sociale et psychologique.
Ce médicament est réservé aux adultes et adolescents âgés de 15 ans ou plus, ayant accepté d'être traités pour leur dépendance aux opioïdes.
Il est disponible sous 2 dosages, à 2 mg et 8 mg de buprénorphine.
Hybride de SUBUTEX mais pas interchangeable
OROBUPRÉ est un médicament hybride de SUBUTEX comprimé sublingual, mais il s'en différencie par sa formulation en lyophilisat oral.
Ces différences de formulation ont pour conséquence des modes d'administration distincts :
- le lyophilisat oral d'OROBUPRÉ est placé sur la langue, et se dissout en 15 secondes environ,
- le comprimé sublingual de SUBUTEX est placé sous la langue et se dissout complètement en 5 à 10 minutes.
Comme le précise l'autorisation de mise sur le marché (AMM), OROBUPRÉ n'est pas interchangeable avec les autres médicaments contenant de la buprénorphine en raison de leur biodisponibilité différente : la dose en mg peut varier entre les produits, exposant le patient à un risque potentiel de surdosage.
Une fois la dose appropriée identifiée pour un patient donné avec un médicament donné, celui-ci ne peut pas être échangé avec une autre forme de buprénorphine.
Pas de bioéquivalence entre OROBUPRÉ et SUBUTEX
Dans son avis du 25 juillet 2018, la Commission de la Transparence a évalué la bioéquivalence entre OROBUPRÉ lyophilisat oral et SUBUTEX comprimé sublingual sur la base de 3 études pharmacocinétiques de phase I [non publiées], monocentriques, à dose unique, randomisées, en ouvert, en cross over (n = 50 volontaires sains) dont :
- deux études de biodisponibilté avec les dosages à 2 mg et 8 mg (RD216/2412719 et RD216/2440120)
- et une étude pivot de bioéquivalence avec le dosage à 8 mg (RD216/2413221).
Ces études de phase I n'ont pas montré de bioéquivalence entre buprénorphine en lyophilisat oral (OROBUPRÉ) et en comprimé sublingual (SUBUTEX) [Cf. Tableaux I et II].
Tableau I - Résultats des études pharmacocinétiques conduites avec la buprénorphine 2 mg et 8 mg en lyophilisat oral (OROBUPRÉ) et en comprimé sublingual (SUBUTEX)
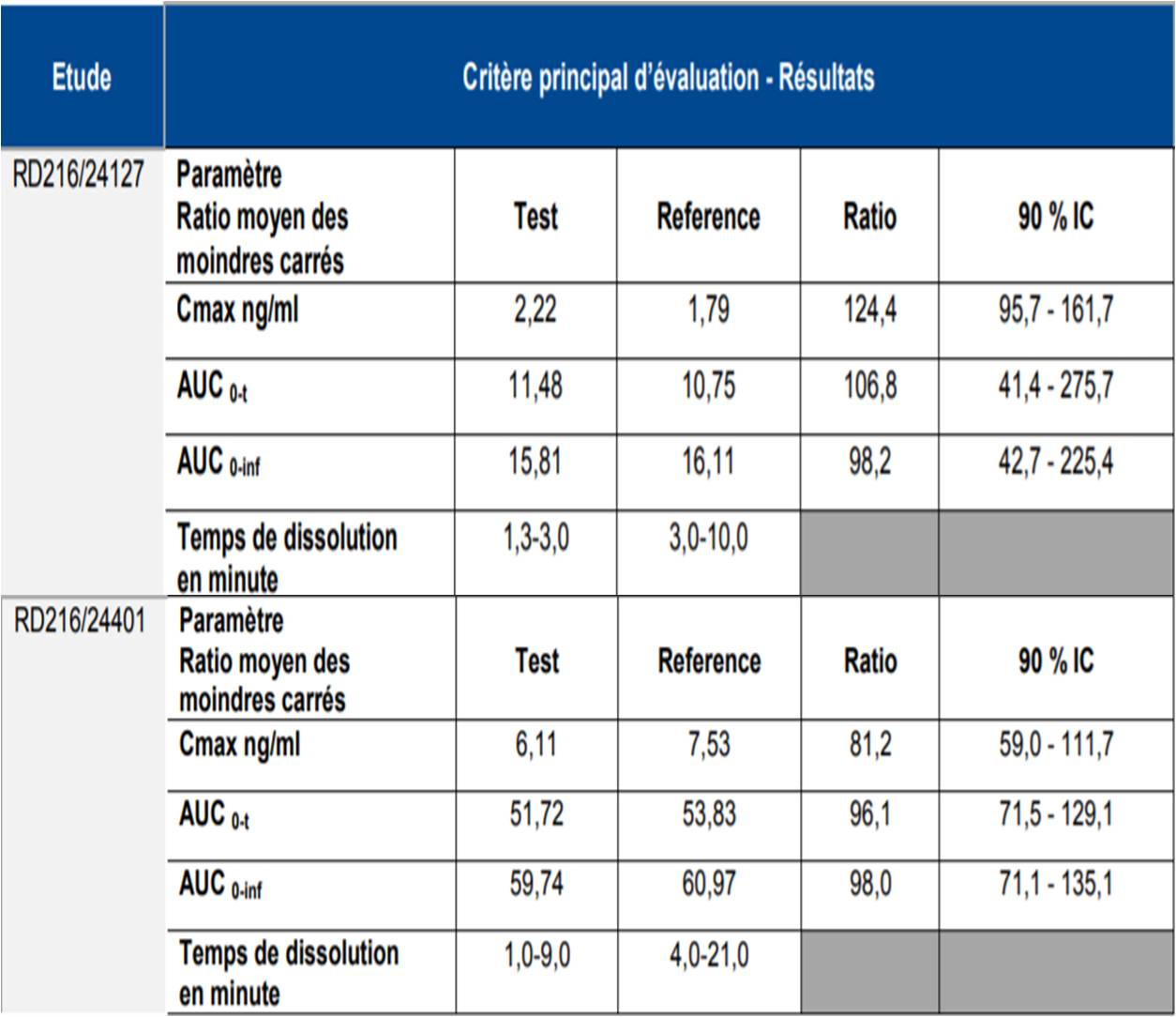
Selon les résultats de l'étude pivot de bioéquivalence (RD216/24132), la biodisponibilité d'OROBUPRÉ a été environ 30 % plus élevée que celle de SUBUTEX (Cf. Tableau II).
Tableau II - Résultats de l'étude pivot de bioéquivalence avec le dosage à 8 mg (RD216/2413221)
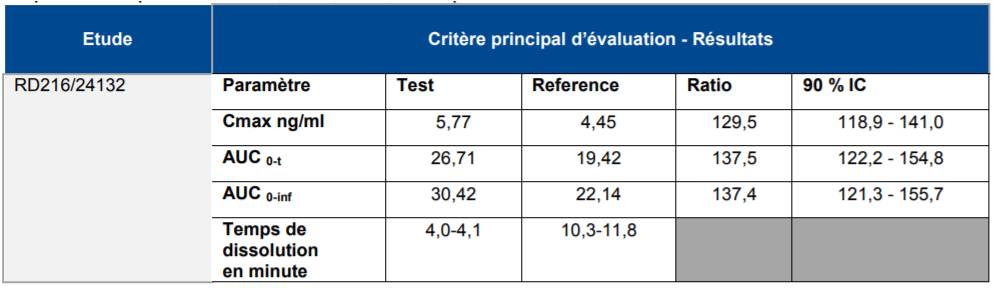
Concernant le temps de dissolution, les résultats de ces études ont suggéré que le lyophilisat OROBUPRÉ se dissout plus rapidement que le comprimé sublingual SUBUTEX, de l'ordre de 2,5 à 2,8 fois plus vite.
En conséquence, OROBUPRÉ lyophilisat oral n'est pas interchangeable avec d'autres médicaments contenant de la buprénorphine (buprénorphine en comprimé sublingual).
Un profil de tolérance similaire à celui de SUBUTEX
La tolérance d'OROBUPRÉ a été évaluée au cours de 2 études cliniques de phase II, randomisées, en ouvert versus SUBUTEX (n = 90 patients adultes dépendants aux opiacés) [Eur Addict Res 2017] :
- l'une multicentrique (étude MD2012/01XP-India), menée en Inde (n = 54 patients),
- l'autre monocentrique (étude MD2012/01XP), conduite au Royaume-Uni (n = 36 patients).
L'évaluation a porté sur la désaturation en oxygène (SpO2) post-dose, le contrôle de la fréquence respiratoire et l'incidence d'effets indésirables reportés (critères de jugement principal).
Selon les résultats de ces études, aucune différence statistiquement significative sur la désaturation en oxygène et la fréquence cardiaque n'a été observée entre les deux médicaments.
S'agissant des effets indésirables (EI) :
- un plus grand nombre d'EI d'intensité légère à modérée liés au médicament ont été rapportés dans le groupe OROBUPRÉ (73,9 %) par rapport au groupe SUBUTEX (30,8 %) dans l'étude réalisée au Royaume-Uni. Ils ont notamment été associés à un syndrome de sevrage (céphalées, arthralgie, rhinorrhée) et à une hypoesthésie (2 cas). Les effets indésirables les plus fréquents ont été des céphalées (4 patients, 17,4 %), des arthralgies (3 patients, 13,0 %), des rhinorrhées (3 patients, 13,0 %) ;
- dans l'étude réalisée en Inde, des cas de prurits plus importants ont été mis en évidence dans le groupe OROBUPRÉ (22 %) par rapport au groupe SUBUTEX (11 %).
Aucun décès ni effets indésirables graves n'ont été rapportés dans ces deux études.
Une "option utile" pour les usagers et les équipes soignantes lors d'une prise supervisée
Sur la base des données disponibles, la Commission de la Transparence a estimé que la place d'OROBUPRÉ 2 mg et 8 mg dans la stratégie thérapeutique est la même que celle de SUBUTEX 2 mg et 8 mg.
Etant donné le temps de dissolution plus rapide, OROBUPRÉ peut permettre un confort d'utilisation et peut représenter une option utile autant pour les usagers que pour les équipes soignantes lors d'une prise supervisée.
A noter que le plus faible dosage d'OROBUPRÉ disponible étant celui à 2 mg, OROBUPRE n'est pas approprié chez les patients stabilisés avec de la buprénorphine sublinguale dosée en dessous de 2 mg.
Au total, la Commission de la Transparence a attribué à OROBUPRÉ un service médical rendu (SMR) modéré, sans amélioration du SMR (ASMR V), compte tenu de l'intérêt pratique de cette formulation lors d'une prise supervisée, mais aussi :
- du fait que les données disponibles reposent sur celles de SUBUTEX comprimé sublingual et sur des données pharmacocinétiques démontrant une non bioéquivalence entre OROBUPRÉ et SUBUTEX,
- de la non interchangeabilité et du risque de confusion entre les deux formulations galéniques,
- des effets indésirables liés au syndrome de sevrage, de l'hypoesthésie et du prurit plus fréquents sous OROBUPRÉ que sous SUBUTEX,
- de l'absence de données sur le risque de mésusage lié à une formulation plus hydrosoluble que celle de SUBUTEX.
Le lyophilisat oral : en pratique
OROBUPRÉ s'administre sur la langue, pour une absorption par la muqueuse buccale.
Une fois le blister ouvert, le lyophilisat oral doit être pris immédiatement.
Sur la langue, le lyophilisat se dissout habituellement en 15 secondes.
Les consignes suivantes doivent être données aux patients :
- éviter de déglutir pendant 2 minutes après la dissolution,
- ne pas consommer d'aliments ou boire durant les 5 minutes qui suivent l'administration.
Si le lyophilisat oral ou la salive contenant de la buprénorphine sont avalés, la buprénorphine sera métabolisée et excrétée et aura un effet minimal.
Plusieurs schémas d'administration possibles
La dose initiale recommandée est 2 mg d'OROBUPRÉ (1 lyophilisat oral OROBUPRÉ 2 mg). En fonction du besoin individuel du patient, une dose supplémentaire de 1 à 2 lyophilisats oraux OROBUPRÉ 2 mg peut être ajoutée le premier jour.
Pendant la phase d'instauration du traitement, il est recommandé de contrôler quotidiennement son administration afin de :
Plusieurs schémas d'administration possibles
La dose initiale recommandée est 2 mg d'OROBUPRÉ (1 lyophilisat oral OROBUPRÉ 2 mg). En fonction du besoin individuel du patient, une dose supplémentaire de 1 à 2 lyophilisats oraux OROBUPRÉ 2 mg peut être ajoutée le premier jour.
Pendant la phase d'instauration du traitement, il est recommandé de contrôler quotidiennement son administration afin de :
- s'assurer du bon usage d'OROBUPRÉ (le lyophilisat doit être placé correctement sur la langue),
- d'observer la réponse du patient au traitement, ce qui permettra d'adapter efficacement la dose administrée en fonction de l'effet clinique obtenu.
Après la phase d'instauration, l'objectif est de stabiliser rapidement le patient.
La posologie peut être ajustée vers le haut ou vers le bas en fonction de l'évaluation de l'état clinique et psychologique du patient par palier de 2 mg à 6 mg, jusqu'à ce que la dose d'entretien efficace minimale soit atteinte.
La posologie maximale est fixée à 18 mg par jour.
Après obtention d'une stabilisation satisfaisante, la fréquence d'administration d'OROBUPRÉ peut être réduite selon 2 schémas :
- une administration tous les 2 jours en doublant la dose quotidienne ajustée individuellement,
- une administration réduite à 3 fois par semaine, en faisant attention de ne jamais dépasser 18 mg par jour.
Après stabilisation, réduire la posologie si possible
Après l'obtention d'une stabilisation satisfaisante évaluée cliniquement et si le patient l'accepte, la posologie peut être réduite progressivement jusqu'à parvenir à une dose d'entretien plus faible.
A noter que le dosage le plus faible d'OROBUPRÉ est 2 mg alors qu'il existe un dosage à 0,4 mg pour SUBUTEX.
Dans certains cas favorables, le traitement peut être arrêté.
Délivrance fractionnée : de quotidienne à hebdomadaire
Comme les autres spécialités de buprénorphine, OROBUPRÉ n'est pas un stupéfiant mais sa prescription et sa délivrance sont très encadrées en raison d'un risque de détournement et de mésusage.
La prescription est établie sur une ordonnance sécurisée, pour 28 jours maximum.
La délivrance est fractionnée par période de 7 jours.
Cependant, pendant la période d'instauration du traitement notamment, une délivrance quotidienne d'OROBUPRÉ est recommandée.
Identité administrative
- Liste I
- Prescription sur ordonnance sécurisée, limitée à 28 jours
- Délivrance fractionnée par périodes de 7 jours
- OROBUPRÉ 2 mg, CIP 3400930123898, prix public TTC = 4,19 euros
- OROBUPRÉ 8 mg, CIP 3400930123874, prix public TTC = 12,87 euros
- Remboursable à 30 % (Journal officiel du 9 octobre 2018, texte 52)
- Agrément aux collectivités (Journal officiel du 9 octobre 2018, texte 53)
- Laboratoire Ethypharm
Pour aller plus loin
Avis de la Commission de la Transparence - OROBUPRE (HAS, 25 juillet 2018)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 7 minutes
7 minutes 1 commentaire
1 commentaire 


Commentaires
Cliquez ici pour revenir à l'accueil.