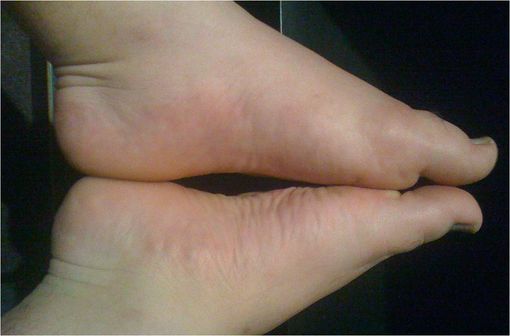
Comparaison entre un pied atteind de goutte et son symétrique, mettant en évidence le gonflement des tissus environnants (illustration @Fatlittlebastard sur Wikimedia).
Arrêt de commercialisation de la seule spécialité française à base de probénécide
Le laboratoire Bouchara-Recordati arrête la commercialisation de BENEMIDE 500 mg comprimé sécable. Ce médicament était en rupture de stock depuis plusieurs semaines.
Seul médicament à base de probénécide (Cf. Encadré 1) commercialisé en France, BENEMIDE dispose d'une autorisation de mise sur le marché (AMM) dans les indications suivantes :
- goutte tophacée ou non en l'absence d'hyperuraturie (Cf. VIDAL Reco "Goutte") ;
- hyperuricémie symptomatique primitive ou secondaire sans insuffisance rénale ;
- adjuvant de la pénicillinothérapie.
Encadré 1 - Le probénécide en bref
| Le probénécide est un agent uricosurique qui inhibe la réabsorption tubulaire des urates par une action enzymatique rapidement réversible d'où son indication dans la goutte ou les hyperuricémies. Inhibiteur de l'excrétion tubulaire de la pénicilline et du PAS, le probénécide permet de maintenir des pénicillinémies élevées, nécessaires au cours du traitement des endocardites d'Osler ou des états septicémiques. C'est pourquoi BENEMIDE est également utilisé comme adjuvant de la pénicillinothérapie. Enfin, le probénécide par voie orale est coadministré avec le cidofovir, un antiviral à usage parentéral commercialisé jusqu'en 2014 sous le nom de VISTIDE 75 mg/mL solution à diluer pour perfusion, dans le traitement de la rétinite à cytomégalovirus chez les sujets atteints de SIDA. Cet antiviral est aujourd'hui disponible en France sous ATU (autorisation temporaire d'utilisation) nominative. Selon le RCP de VISTIDE, chaque perfusion de cidofovir doit s'accompagner d'une préhydratation par injection intraveineuse de sérum physiologique et de l'administration de probénécide par voie orale pour minimiser les risques potentiels de néphrotoxicité. Cette utilisation n'était pas prévue dans l'AMM de BENEMIDE. |
Importation de PROBENECIDE BIOKANOL pour couvrir les besoins du marché français
Afin de maintenir l'approvisionnement du marché français en probénécide, l'Agence nationale de sécurité du médicament et des produits de santé (ANSM) a autorisé, à titre exceptionnel et transitoire, l'importation de PROBENECIDE BIOKANOL 500 mg comprimé sécable (Cf. RCP et notice), une spécialité initialement destinée au marché allemand.
La distribution de ce médicament importé est limitée aux pharmacies hospitalières. La rétrocession aux patients ambulatoires est possible.
L'exploitation de PROBENECIDE BIOKANOL est assurée par le laboratoire INRESA.
Aucune information n'est disponible à ce jour quant à la durée de cette situation.
Utilisation de PROBENECIDE BIOKANOL : "évaluer au cas par cas le bénéfice et le risque"
Dans une lettre aux professionnels de santé, le laboratoire INRESA indique que "Le prescripteur et/ou le dispensateur doivent tenir compte des différences éventuelles entre le médicament importé et le médicament manquant habituellement prescrit, évaluer au cas par cas le bénéfice et le risque de l'utilisation d'une spécialité différente dans ce contexte" (Cf. RCP de BENEMIDE versus RCP de PROBENECIDE BIOKANOL).
De même composition qualitative et quantitative en probénécide, correspondant à 500 mg par unité de prise, et de forme galénique identique, BENEMIDE et PROBENECIDE BIOKANOL diffèrent, entre autres :
- par leur composition en excipients avec la présence d'amidon de blé dans la spécialité française et non dans la spécialité allemande ;
- par leurs modalités d'administration chez l'enfant :
- les comprimés sécables de PROBENECIDE BIOKANOL doivent être pris au cours du repas sans être mâchés, avec beaucoup de liquide ;
- les comprimés de BENEMIDE doit être impérativement écrasés et dissous dans un peu de yaourt ou de liquide sucré chez l'enfant de moins de 6 ans.
Pour aller plus loin
BENEMIDE 500 mg, comprimé sécable - Arrêt de commercialisation (21 décembre 2016)
Lettre du laboratoire aux professionnels de santé (sur le site de l'ANSM, 21 décembre 2016)
Notice en français de PROBENECID BIOKANOL 500 mg comprimé sécable
RCP en français de PROBENECID BIOKANOL 500 mg comprimé sécable
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.