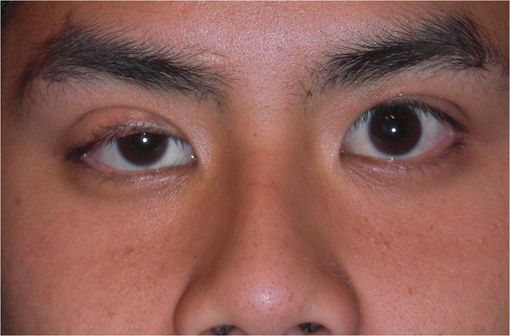
Ptosis de la paupière droite, avec rétraction compensatrice de la paupière gauche, chez un homme atteint d'une myasthénie (illustration @Andrewya, sur Wikimedia).
Nouvelle formulation à libération prolongée en complément de la formulation à libération immédiate
MESTINON LP 180 mg comprimé à libération prolongée est une nouvelle présentation à base de bromure de pyridostigmine (Cf. Encadré 1) en complément de la formulation à libération immédiate MESTINON 60 mg comprimé enrobé déjà commercialisée, dans le traitement de la myasthénie.
Encadré 1 - Le bromure de pyridostigmine et sa formulation LP en bref
| Dans la myasthénie, le bromure de pyridostigmine est utilisé pour ses propriétés anticholinestérasiques. Il prolonge et augmente les effets muscariniques et nicotiniques de l'acétylcholine à savoir l'intensité et le rythme des contractions des fibres musculaires. Les comprimés de MESTINON LP 180 mg se composent d'une matrice insoluble formée de cire de carnauba et d'agents agissant sur la dissolution. Cette formulation galénique permet d'obtenir une libération prolongée du principe actif avec une demi-vie plasmatique d'environ 4 à 6 heures alors que celle de la formulation à libération immédiate est de 2 heures. |
Cette nouvelle présentation LP est indiquée dans la myasthénie grave non équilibrée avec la forme à libération immédiate.
Elle n'est pas adaptée au traitement des crises myasthéniques et, à la différence de la formulation à libération immédiate, n'est pas indiquée dans le traitement de l'atonie intestinale.
MESTINON LP 180 mg était disponible en France depuis 1993 sous ATU (autorisation temporaire d'utilisation) nominative, avant d'obtenir un AMM (autorisation de mise sur le marché) en juin 2015.
Une autre formulation de MESTINON en sirop à 60 mg/5 mL est toujours inscrite sous le statut d'ATU nominative (source ANSM, ATUn inscrites au 1er semestre 2016).
Efficacité et tolérance de MESTIMON 180 mg LP : une étude observationnelle avant/après
L'évaluation de l'efficacité et de la tolérance de MESTINON LP 180 mg reposent sur une étude observationnelle prospective comparative avant/après instauration du traitement par MESTINON LP 180 mg (Sieb JP & Köhler W. Clinical Neurology and Neurosurgery 2010).
Soixante douze patients ont été inclus dans l'étude. Tous avaient été précédemment traités par MESTINON 60 mg.
Les résultats de cette étude ont montré qu'un mois après l'instauration du traitement par MESTINON LP 180 mg (swich), la gravité de la myasthénie s'était améliorée de manière significative, avec une diminution du score de Besinger (Cf. Encadré 2) de 0,9 ± 0,5 à 0,6 ± 0,4 (p < 0,001).
Elle n'est pas adaptée au traitement des crises myasthéniques et, à la différence de la formulation à libération immédiate, n'est pas indiquée dans le traitement de l'atonie intestinale.
MESTINON LP 180 mg était disponible en France depuis 1993 sous ATU (autorisation temporaire d'utilisation) nominative, avant d'obtenir un AMM (autorisation de mise sur le marché) en juin 2015.
Une autre formulation de MESTINON en sirop à 60 mg/5 mL est toujours inscrite sous le statut d'ATU nominative (source ANSM, ATUn inscrites au 1er semestre 2016).
Efficacité et tolérance de MESTIMON 180 mg LP : une étude observationnelle avant/après
L'évaluation de l'efficacité et de la tolérance de MESTINON LP 180 mg reposent sur une étude observationnelle prospective comparative avant/après instauration du traitement par MESTINON LP 180 mg (Sieb JP & Köhler W. Clinical Neurology and Neurosurgery 2010).
Soixante douze patients ont été inclus dans l'étude. Tous avaient été précédemment traités par MESTINON 60 mg.
Les résultats de cette étude ont montré qu'un mois après l'instauration du traitement par MESTINON LP 180 mg (swich), la gravité de la myasthénie s'était améliorée de manière significative, avec une diminution du score de Besinger (Cf. Encadré 2) de 0,9 ± 0,5 à 0,6 ± 0,4 (p < 0,001).
Encadré 2 - Le score de Besinger
|
Le score de Besinger est un score clinique composé de huit critères visant à évaluer au moyen de tests fonctionnels la gravité de la myasthénie :
|
La qualité de vie des patients s'est également améliorée de manière significative avec une augmentation du score au questionnaire EuroQoL de 0,626 ± 0,286 à 0,782 ± 0,186 (p < 0,001).
En termes de tolérance, les effets indésirables décrits depuis la mise à disposition de MESTIMNON 180 mg LP en 1993 (ATU nominative), sont notamment :
En termes de tolérance, les effets indésirables décrits depuis la mise à disposition de MESTIMNON 180 mg LP en 1993 (ATU nominative), sont notamment :
- des effets muscariniques : crampes abdominales, nausées et vomissements, diarrhées, hypersalivation, augmentation des sécrétions bronchiques, péristaltiques et lacrymales, bradycardie, myosis ;
- des effets nicotiniques : crampes musculaires, fasciculations, soubresauts musculaires et faiblesse musculaire.
La diminution de la posologie permet en général de les faire disparaître.
L'efficacité de MESTINON LP 180 mg n'a pas été comparée à celle MESTINON 60 mg.
Sur la base des données disponibles, la Commission de la transparence a considéré que MESTINON LP 180 mg apportait un SMR (service médical rendu) important dans le traitement de 2e intention des patients avec myasthénie grave non équilibrée avec la forme à libération immédiate (Cf. Avis du 20 janvier 2016).
MESTINON LP 180 mg en pratique
L'efficacité de MESTINON LP 180 mg n'a pas été comparée à celle MESTINON 60 mg.
Sur la base des données disponibles, la Commission de la transparence a considéré que MESTINON LP 180 mg apportait un SMR (service médical rendu) important dans le traitement de 2e intention des patients avec myasthénie grave non équilibrée avec la forme à libération immédiate (Cf. Avis du 20 janvier 2016).
MESTINON LP 180 mg en pratique
- Adapter la posologie de manière individuelle
La posologie doit être adaptée aux besoins individuels de chaque patient.
La dose habituellement utilisée est de 1 à 2 comprimés par jour.
Pour assurer une couverture thérapeutique sur l'ensemble du nycthémère, les comprimés de MESTINON LP 180 mg peuvent être associés à la prise de comprimés de MESTINON 60 mg.
MESTINON LP 180 mg n'est pas recommandé chez l'enfant de moins de 15 ans.
La dose habituellement utilisée est de 1 à 2 comprimés par jour.
Pour assurer une couverture thérapeutique sur l'ensemble du nycthémère, les comprimés de MESTINON LP 180 mg peuvent être associés à la prise de comprimés de MESTINON 60 mg.
MESTINON LP 180 mg n'est pas recommandé chez l'enfant de moins de 15 ans.
- En cas de maladie respiratoire obstructive : prudence extrême
MESTINON LP 180 mg est contre-indiqué en cas d'asthme, de maladie de Parkinson ou d'obstruction mécanique des voies digestives et urinaires.
Selon les termes du RCP (résumé des caractéristiques du produit), une prudence extrême est recommandée en cas de maladies obstructives respiratoires telles qu'un asthme bronchique et des bronchopneumopathies chroniques obstructives (BPCO).
Identité administrative
Selon les termes du RCP (résumé des caractéristiques du produit), une prudence extrême est recommandée en cas de maladies obstructives respiratoires telles qu'un asthme bronchique et des bronchopneumopathies chroniques obstructives (BPCO).
Identité administrative
- Liste I
- Boîte de 50, CIP 3400930017586
- Remboursable à 65 % (Journal officiel du 29 septembre 2016 - texte 33)
- Prix public TTC = 115,20 euros
- Agrément aux collectivités (Journal officiel du 29 septembre 2016 - texte 34)
- Laboratoire Meda Pharma
Pour aller plus loin
Avis de la Transparence (HAS, 20 janvier 2016)
Sieb JP & Köhler W. Benefits from sustained-release pyridostigmine bromide in myasthenia gravis : results of a prospective multicenter open-label trial. Clinical Neurology and Neurosurgery 2010 ; 112 : 781–784.
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.