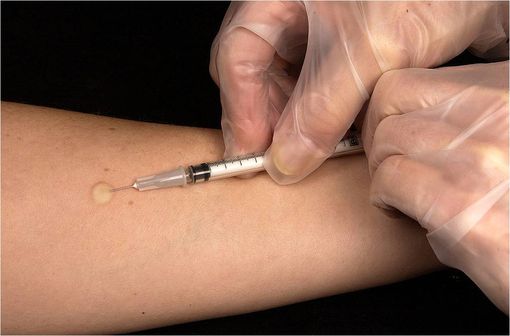
Intradermoréaction à la tuberculine ou test Mantoux, pour le dépistage de la tuberculose (illustration @ Greg Knobloch, CDC, sur Wikimedia).
Les données épidémiologiques disponibles sur la tuberculose sont rassurantes en France avec une diminution régulière du nombre de cas déclarés (moins de 5000 cas par an depuis 2010) et une incidence qui devrait rapidement descendre en dessous de 7 cas pour 100 000 habitants.
Mais, à l'échelon mondial, la tuberculose reste une cause majeure de morbi-mortalité, malgré l'avènement de progrès considérables.
En effet, l'Organisation mondiale de la santé (OMS) évalue en 2014 à 9,6 millions le nombre de nouveaux cas et à 1,5 million le nombre de décès.
Les ambitions sont de réduire à l'horizon 2030 l'incidence de la maladie de 90 % et le nombre de décès de 95 %. Cependant, pour l'OMS, une quasi élimination est possible dans 33 pays, dont la France.
L'"infection tuberculeuse latente" : nouvelle entité, nouvelle stratégie thérapeutique
A l'aune de cet ambitieux objectif de Santé publique, la classification entre l'infection tuberculeuse active et l'infection tuberculeuse latente, qui restait obscure pour beaucoup, a été clarifiée.
Ainsi, la tuberculose-maladie désigne logiquement l'infection active, avec des signes cliniques et/ou radiologiques, dont le traitement antibiotique est indispensable.
La tuberculose-infection, désormais dénommée "infection tuberculeuse latente - ITL", correspond au stade latent de l'infection, sans symptomatologie clinique, ni anomalie radiologique.
Son diagnostic repose sur l'intradermoréaction à la tuberculine (IDR) et/ou sur les tests IGRA (Interferon Gamma Release Assay) [Voir l'Avis relatif à l'utilisation des tests de détection de la production d'interféron-gamma, HCSP 1er juillet 2011].
La prise en charge de l'ITL a fait l'objet en 2015 de directives spécifiques de l'OMS (voir Directives pour la prise en charge de l'infection tuberculeuse latente (ITL) - OMS, 2015), synthétisées sous la forme d'un arbre décisionnel dans la Reco VIDAL "Tuberculose pulmonaire" (voir Figure 1).
(extrait de la Reco VIDAL "Tuberculose pulmonaire")
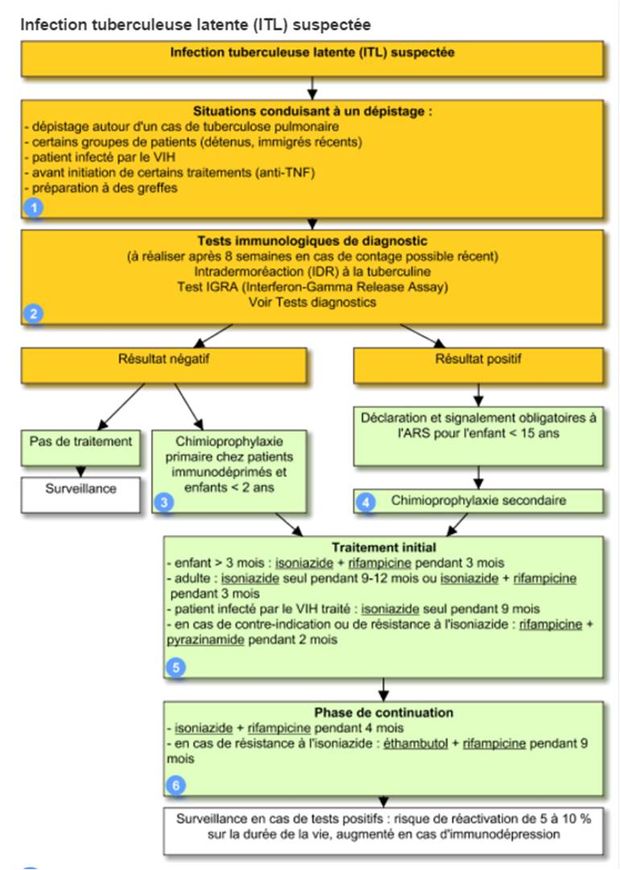
Les pastilles bleues renvoient à des commentaires figurant dans le texte de la Reco VIDAL.
Pas de nouveaux médicaments mais de nouvelles stratégies thérapeutiques
Pour concourir à cet objectif, outre le dépistage et l'isolement des cas contagieux, les médicaments des tuberculoses à bacilles de Koch (BK) sensibles, s'ils n'ont guère changé et datent tous de plus de 35 ans, font l'objet de nouvelles stratégies thérapeutiques où les posologies ont notamment été modifiées et optimisées : elles sont précisées dans la Reco VIDAL "Tuberculose pulmonaire" (lien direct ici).
Résistance multiple, ultrarésistance : une classification précisée
Les BK multirésistants sont une préoccupation du fait des difficultés thérapeutiques qu'ils représentent.
A ce jour, en France, le taux observé est faible, autour de 2 %, soit une centaine de cas.
Les causes essentielles d'acquisition de ces résistances sont des traitements précédents mal conduits, mais surtout une mauvaise observance des patients. L'essentiel des cas s'observe chez des sujets qui ont déjà été traités, très souvent originaires d'autre pays, en particulier ceux de l'ex-URSS.
La classification de ces résistances est précisée de la manière suivante :
- Multi Drug Resistant Tuberculosis ou MDR
On parle de MDR pour des souches ayant acquis une résistance aux deux antituberculeux de 1re ligne : isoniazide et rifampicine.
En 2012, en France, le chiffre des MDR à l'association isoniazide + rifampicine était de 2,3 % pour des patients jamais traités, mais de 8,8 % pour des patients ayant déjà été traités.
- Ultrarésistance ou eXtensively Drug-Resistant Tuberculosis (XDR-TB)
L'XDR-TB est définie par une résistance à d'autres molécules que l'isoniazide et la rifampicine, au minimum une fluoroquinolone et un des médicaments injectables suivants : kanamycine, amikacine, ou capréomycine (CAPASTAT 1 g/10 ml solution injectable, disponible sous autorisation temporaire d'utilisation nominative, ATUn, depuis 2009).
Le traitement est long, de 18 à 24 mois, et nécessite souvent 5 molécules actives.
Il en existe une dizaine dont la plus récente est la bédaquiline (SIRTURO), une diarylquinoline qui vient d'obtenir une autorisation de mise sur le marché (AMM) européenne conditionnelle (voir Résumé des caractéristiques du produit de SIRTURO sur le site de l'Agence européenne du médicament).
La prescription de ces traitements, à l'aide d'un antibiogramme, relève de milieux spécialisés. Elle doit être instaurée et surveillée par un médecin expérimenté dans la prise en charge de la tuberculose multirésistante.
En conclusion
La conclusion essentielle, qui n'est pas du tout une nouveauté, est que plus que jamais il faut insister sur l'importance de l'observance au traitement.
La Reco VIDAL "Tuberculose pulmonaire" propose une synthèse actualisée de la stratégie thérapeutique désormais recommandée pour faire face à l'évolution épidémiologique de cette infection et aux résistances aux médicaments antituberculeux, sous forme notamment d'arbres décisionnels que vous pouvez consulter en ligne sur VIDAL.fr (lien direct ici).
Pour aller plus loin
VIDAL Reco "Tuberculose pulmonaire" sur VIDAL.fr
Directives pour la prise en charge de l'infection tuberculeuse latente (ITL) - OMS, 2015
Avis relatif à l'utilisation des tests de détection de la production d'interféron-gamma », HCSP 1er juillet 2011
Résumé des caractéristiques du produit de SIRTURO, sur le site de l'Agence européenne du médicament
- AMIKACINE B. BRAUN 10 mg/ml sol p perf
- AMIKACINE B. BRAUN 2,5 mg/ml sol p perf
- AMIKACINE B. BRAUN 5 mg/ml sol p perf
- ANSATIPINE 150 mg gél
- DEXAMBUTOL 500 mg cp pellic
- MYAMBUTOL 1000 mg/10 ml sol inj
- MYAMBUTOL 400 mg cp pellic séc
- PIRILENE 500 mg cp
- RIFADINE 2 pour cent susp buv
- RIFADINE 300 mg gél
- RIFADINE 600 mg pdre/solv p sol p perf IV
- RIFATER cp enr
- RIFINAH 300 mg/150 mg cp enr
- RIMACTAN 300 mg gél
- TUBERTEST sol inj

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.