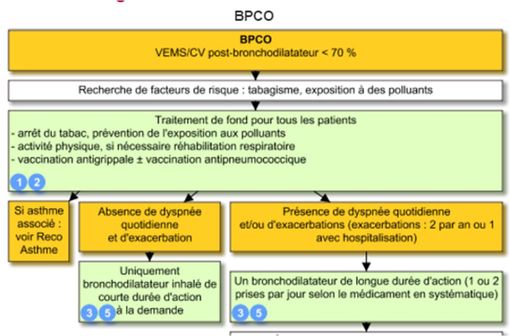
Extrait de l'arbre décisionnel VIDAL Reco "BPCO" (illustration).
STRIVERDI RESPIMAT (olodatérol) est un nouveau bronchodilatateur bêta-2 agoniste de longue durée d'action, administré par le dispositif inhalateur RESPIMAT.
Il se présente sous forme de solution pour inhalation à 2,5 µg/dose en cartouche de 4 ml (60 doses).
STRIVERDI RESPIMAT est indiqué dans le traitement bronchodilatateur continu de la bronchopneumopathie chronique obstructive (BPCO).
Son principe actif, l'olodatérol, présente une affinité et une sélectivité élevées pour les récepteurs ß2-adrénergiques humains, exprimés principalement au niveau des muscles lisses des voies respiratoires.
Il est caractérisé par un début d'action rapide et une durée d'action d'au moins 24 heures.
Une efficacité démontrée en terme de variation du VEMS post-dose versus placebo
L'efficacité de l'olodatérol 5 µg/jour a principalement été démontrée sur la base de 4 études de protocoles identiques deux à deux, randomisées en double aveugle versus placebo (études 1222.11 et 1222.12) ou versus placebo et versus formotérol(*) 12 µg x 2 /jour (études 1222.13 et 1222.14), d'une durée de 48 semaines chez des patients atteints de BPCO modérée (stade II) à très sévère (stade IV).
(*) Le formotérol est un bronchodilatateur bêta-2 mimétique de longue durée d'action par voie inhalée.
Les patients pouvaient prendre des traitements concomitants (anticholinergiques de courte et de longue durée d'action, corticoïdes inhalés, salbutamol) et, en cas d'exacerbation, pouvaient être traités par salbutamol, corticoïdes oraux, dérivés de la théophylline et antibiotiques.
Les co-critères de jugements principaux communs aux 4 études étaient l'aire sous la courbe du VEMS entre 0 et 3 heures post-dose (ASC0-3h) et la variation du VEMS pré-dose par rapport à la valeur initiale, évaluées après 12 semaines de traitement pour les 2 études versus placebo et après 24 semaines de traitement pour les 2 études versus formotérol et placebo.
Le score de dyspnée (score focal TDI) à 24 semaines était le 3e co-critère de jugement principal des 2 études versus formotérol et placebo.
Selon l'avis de la Commission de la transparence (18 mars 2015), ces 4 études ont montré que l'olodatérol 5 µg/jour était efficace par rapport au placebo sur l'ASC0-3h ainsi que sur la diminution de consommation de traitements de secours (- 0,956 bouffées de traitement de secours/jour), mais pas en terme d'évolution du VEMS pré-dose (< 100 ml, différence non cliniquement pertinente).
Pas de réduction des exacerbations, ni de la dyspnée par rapport au placebo
Ces études n'ont pas permis de démontrer que l'olodatérol était supérieur au placebo en termes de réduction des exacerbations de la BPCO, de réduction de la dyspnée (différence non significative) ou d'amélioration de la qualité de vie (différence non cliniquement pertinente).
Dans les études versus comparateur actif, aucune différence significative n'a été observée par rapport au formotérol 12 µgx 2/jour sur les critères étudiés (ASC0-3h du VEMS, variation du VEMS pré-dose et dyspnée) et la non-infériorité de l'olodatérol 5 µg/jour par rapport au formotérol 12 µgx 2/jour n'a pas été évaluée.
Des données à visée exploratoire versus tiotropium (anticholinergique antimuscarinique) et indacaterol (bêta-2-agoniste de longue durée d'action) n'ont pas non plus permis de démontrer la non-infériorité de l'olodatérol par rapport à ces traitements symptomatiques continus de la BPCO, dans des populations de patients comparables.
En terme de tolérance, l'olodatérol a été bien toléré.
Les effets indésirables rapportés avec l'olodatérol dans les études cliniques ont été peu fréquents (>= 1/1000 à <1/100) et non graves, principalement à type de rhinopharyngite, sensations vertigineuses et éruption cutanée.
Le risque d'effets systémiques, en particulier cardio-vasculaires, propres à la classe des bêta-2 agonistes de longue durée d'action, doit toutefois être pris en considération.
Un service médical rendu "modéré"
Considérant l'ensemble des données fournies par le laboratoire Boehringer Ingelheim, la Commission de la transparence (CT) a positionné STRIVERDI RESPIMAT dans la stratégie thérapeutique de la BPCO comme "traitement symptomatique continu de la BPCO chez les patients dont la gêne respiratoire est devenue permanente, c'est-à-dire lorsque les symptômes persistent malgré l'utilisation d'un bronchodilatateur de courte durée d'action", le traitement ne devant être poursuivi que si le patient en ressent un bénéfice.
Elle a précisé qu'"aucune donnée ne permet de situer l'olodatérol par rapport à ses comparateurs cliniquement pertinents".
Concluant à un rapport efficacité/effets indésirables moyen, la CT a considéré que le service médical rendu (SMR) par STRIVERDI RESPIMAT est modéré dans son indication d'autorisation de mise sur le marché.
STRIVERDI RESPIMAT : en pratique
STRIVERDI RESPIMAT s'utilise par voie inhalée exclusivement.
La cartouche contenant la solution pour inhalation ne peut être utilisée qu'avec l'inhalateur RESPIMAT.
La posologie recommandée chez l'adulte est de 5 µg d'olodatérol, soit 2 bouffées en une prise par jour, à heure fixe dans la journée, sans dépasser cette posologie.
Aucune adaptation posologique n'est nécessaire chez les sujets âgés, les patients en insuffisance hépatique légère à modérée ou en cas d'insuffisance rénale.
STRIVERDI RESPIMAT ne doit pas être utilisé chez les patients asthmatiques.
Comme avec les autres agonistes bêta-2 adrénergiques, il peut être nécessaire d'interrompre le traitement chez certains patients présentant des effets cardiovasculaires significatifs tels des augmentations de la fréquence cardiaque, de la pression artérielle et/ou des symptômes cliniques.
Les instructions destinées aux patients pour l'utilisation et la manipulation sont détaillées dans la monographie VIDAL de STRIVERDI RESPIMAT.
Pour une administration correcte du médicament, le médecin ou le professionnel de santé devra s'assurer du bon usage de l'appareil par le patient.
Après insertion de la cartouche dans l'inhalateur, STRIVERDI RESPIMAT se conserve 3 mois.
Il ne doit pas être congelé.
Identité administrative
LISTE I
STRIVERDI RESPIMAT 2,5 µg/dose, 1 cartouche de 60 doses et 1 inhalateur RESPIMAT, CIP 3400927723278
Prix public : 31,10 € TTC
Remboursement à 30 % (Journal officiel du 15 octobre 2015 - texte 30)
Agrément aux collectivités (Journal officiel du 15 octobre 2015 - texte 31)
Laboratoire Boehringer Ingelheim France
Pour aller plus loin
Avis de la Commission de la Transparence (HAS, 18 mars 2015)
Consulter VIDAL Reco "BPCO"
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.