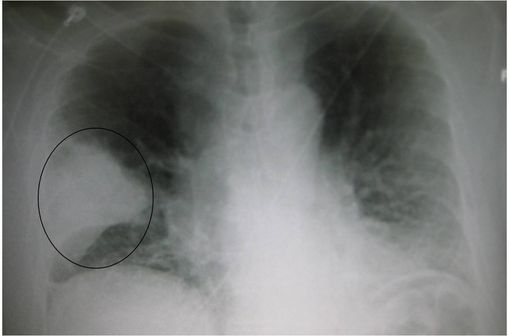
Radiographie de thorax montrant une pneumonie franche lobaire aiguë en forme de coin dans le poumon droit (illustration @ Dr James Heilman, sur Wikimedia).
MABELIO 500 mg poudre pour solution à diluer pour solution pour perfusion est indiqué dans le traitement des infections suivantes chez l'adulte :
- pneumonies nosocomiales (PN), à l'exclusion des pneumonies acquises sous ventilation mécanique (PAVM) ;
- pneumonies communautaires (PC) (voir la Reco VIDAL "Pneumonie communautaire aiguë de l'adulte").
Le principe actif de MABELIO, le ceftobiprole est une nouvelle substance de la famille des (autres) céphalosporines.
Ce médicament fait l'objet d'une surveillance supplémentaire qui permettra l'identification rapide de nouvelles informations relatives à la sécurité. Les professionnels de santé déclarent tout effet indésirable suspecté.
Place dans la stratégie thérapeutique
Selon l'avis de la Commission de la transparence du 28 mai 2014, dans l'indication "Traitement des pneumonies nosocomiales sauf les pneumonies acquises sous ventilation mécanique", "MABELIO serait plus particulièrement réservé aux patients requérant un traitement par voie intra-veineuse, en cas d'infections à bactéries multi-résistantes (Staphylococcus aureus méti-R (SARM : NDLR), Streptococcus pneumoniae péni-R) sensibles au ceftobiprole et lorsqu'il n'existe aucune alternative thérapeutique ou lorsque les autres alternatives thérapeutiques ne peuvent être utilisées".
Dans le contexte actuel de besoin de médicaments nouveaux actifs sur des bactéries résistantes, la Commission de la transparence précise par ailleurs que "le ceftobiprole (MABELIO) actif au moins in vitro sur des germes résistants tels que le SARM, constitue une nouvelle option thérapeutique, en réponse à ce besoin thérapeutique identifié"
Dans le traitement des pneumonies communautaires, la Commission de la transparence considère que "le ceftobiprole n'a pas de place au regard des alternatives thérapeutiques existantes plus simples d'emploi et de spectre plus étroit, d'autant plus qu'il manque des données sur l'efficacité dans les pneumonies communautaires à SARM (Staphylococcus aureus méti-R) et vis-à-vis des souches de S. pneumoniae non sensibles à la pénicilline."
MABELIO en pratique
MABELIO est administré par voie intraveineuse.
Présenté en poudre, MABELIO doit préalablement être reconstitué puis dilué avant d'être injecté :
- La reconstitution est réalisée avec de l'eau stérile pour préparations injectables ou une solution de dextrose 50 mg/ml (5 %). Après reconstitution, chaque ml de concentré contient 50 mg de ceftobiprole (sous forme de 66,7 mg de ceftobiprole médocaril sodique).
- La dilution est réalisée avec une solution de chlorure de sodium 9 mg/ml (0,9 %) pour préparations injectables, ou une solution de dextrose 50 mg/ml (5 %) pour préparations injectables, ou une solution de Ringer lactate pour préparations injectables. MABELIO et les solutions contenant du calcium ne doivent pas être mélangés ni administrés simultanément sur la même ligne intraveineuse en raison d'un risque de précipitation.
- Avant reconstitution, MABELIO doit être conservé au réfrigérateur, entre 2 °C et 8°C, dans son emballage et à l'abri de la lumière.
La dose recommandée de MABELIO est de 500 mg, administrée par perfusion intraveineuse de 2 heures, toutes les 8 heures.
Un ajustement posologique (diminution de la dose, allongement du délai entre chaque perfusion ou de la durée de perfusion) est nécessaire en cas d'insuffisance rénale (en fonction de la clairance de la créatinine).
Pour la pneumonie communautaire (PC), le relais par un antibiotique adapté administré par voie orale peut être envisagé après au moins 3 jours de traitement par ceftobiprole médocaril sodique administré par voie intraveineuse, selon la réponse clinique du patient.
Identité administrative
- Liste I
- Prescription hospitalière
- Boîte de 10 flacons de 20 ml, CIP 3400927731662
- Agrément aux collectivités dans le "traitement chez l'adulte des pneumonies nosocomiales, à l'exclusion des pneumonies acquises sous ventilation mécanique"
- Laboratoire Novex Pharma
Pour aller plus loin
Avis de la Commission de la Transparence (HAS, 28 mai 2014)
Arrêté du 29 septembre 2014 portant inscription de MABELIO à l'agrément aux collectivités (Journal officiel du 1er octobre 2014)
La monographie en lien ci-dessous est en cours de mise à jour concernant les informations contenues dans cette actualité à la date de sa publication.
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.