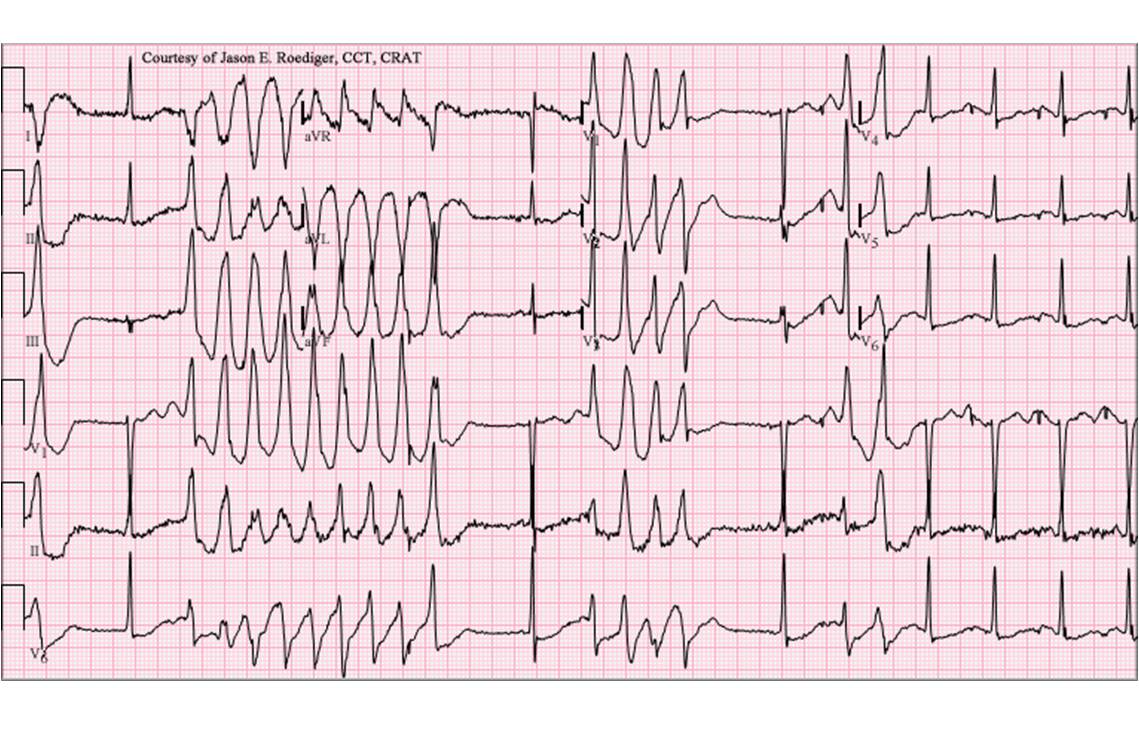
Le syndrome du QT long est associé à un risque élevé de torsades de pointe (ECG ci-dessous) ou de fibrillation ventriculaire (illustration @ Jer5150, Wikimedia).
En 2010, les données de pharmacovigilance avaient montré un risque d'allongement des espaces QT et PR chez les patients sous INVIRASE (saquinavir), conduisant le laboratoire Roche, en accord avec l'EMA (Agence européenne du médicament) et l'ANSM (Agence nationale de sécurité du médicament et des produits de santé), à recommander un contrôle électrocardiographique avant l'instauration du traitement et pendant le suivi.
Dans un communiqué de l'ANSM du 27 mai 2014, ces recommandations ont été actualisées afin de prendre en compte les résultats d'une nouvelle étude de pharmacocinétique :
- lors de l'instauration d'un traitement par INVIRASE chez des patients naïfs de traitement antirétroviral, en plus de l'ECG pratiqué avant le début du traitement, un ECG doit être dorénavant fait après environ 10 jours de traitement, c'est-à-dire au moment où l'allongement de l'intervalle QTcF (espace QT corrigé en fonction de la fréquence cardiaque selon la formule de Fredericia : QTcF = QT/RR) atteint son maximum ;
- chez ces patients, le traitement par INVIRASE doit continuer à être instauré à dose réduite, soit 500 mg 2 fois par jour pendant les 7 premiers jours, avant de passer à la dose standard de 1 000 mg 2 fois par jour, en association au ritonavir 100 mg deux fois par jour et d'autres antirétroviraux.
Pour les patients en cours de traitement par INVIRASE/ritonavir (1 000/100 mg 2 fois par jour), les modalités de surveillance électrocardiographique ne sont pas modifiées.
Le résumé des caractéristiques du produit (RCP) des médicaments INVIRASE a été modifié pour intégrer ces nouvelles modalités de surveillance.
A propos de l'étude
Dans la lettre du laboratoire aux professionnels de santé, il est précisé que l'étude sur laquelle repose ces nouvelles recommandations est une étude ouverte réalisée chez 23 patients infectés par le VIH-1 et naïfs de traitement antirétroviral. Les patients ont reçu :
- les 7 premiers jours, saquinavir/ritonavir 500/100 mg 2 fois par jour associé à la prise de 2 inhibiteurs nucléosidiques de la transcriptase inverse (INTI) ;
- les 7 jours suivants, saquinavir/ritonavir 1 000 /100 mg 2 fois par jour associé à la prise de 2 INTI.
Pour mémoire
INVIRASE 200 mg gélule et INVIRASE 500 mg comprimé pelliculé sont indiqués dans le traitement des patients adultes infectés par le VIH-1.
Ils doivent être administrés uniquement en association avec le ritonavir et avec d'autres médicaments antirétroviraux.
Pour aller plus loin
Invirase (saquinavir) : Actualisation des recommandations électrocardiographiques - Lettre aux professionnels de santé (ANSM, 27 mai 2014)
Lettre du laboratoire Roche aux professionnels de santé (sur le site de l'ANSM, 27 mai 2014)
Sur www.vidal.fr
INVIRASE, associé à un risque arythmogène (3 septembre 2010)
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 2 minutes
2 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.