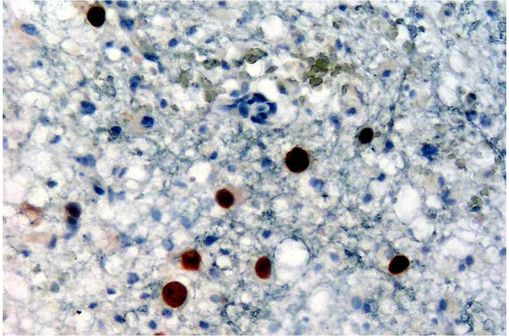
Détection immunohistochimique de la protéine du virus JC (tâches brunes) sur une biopsie cérébrale réalisée dans un contexte de LEMP (illustration @ Marvin 101 sur Wikimedia).
Conformément à la recommandation du PRAC (Comité pour l'évaluation des risques en matière de pharmacovigilance), l'ANSM (Agence nationale de sécurité du médicament et des produits de santé) informe les professionnels de santé de la notification d'un cas fatal de LEMP (leucoencéphalopathie multifocale progressive) survenu en octobre chez une patiente allemande traitée par TECFIDERA (diméthyl fumarate) pour une sclérose en plaques.
Pour rappel, la LEMP est une pathologie infectieuse grave touchant le système nerveux central et pouvant être fatale ou entraîner un handicap sévère. Il s'agit d'une infection opportuniste liée à la réactivation d'un virus, le virus JC.
Premier cas de LEMP
La patiente était traitée depuis 4,5 ans et présentait une lymphopénie sévère chronique depuis plus de 3,5 ans. La lymphopénie est un effet indésirable possible et connu de TECFIDERA. Dans les essais cliniques, le nombre de lymphocytes a été réduit d'environ 30 %.
La patiente est décédée des complications liées à la détérioration de son état neurologique et à une pneumopathie d'inhalation.
Il s'agit du premier cas de LEMP associé à TECFIDERA. D'autres cas de LEMP ont été précédemment rapportés avec l'utilisation d'esters de l'acide fumarique chez des patients lymphopéniques atteints de psoriasis mais, dans la majorité de ces cas, le lien de causalité n'a pu être clairement identifié (du fait de la présence d'autres facteurs de risque de LEMP associés).
Surveillance par hémogramme
Il est rappelé qu'une surveillance étroite des patients sous TECFIDERA est nécessaire.
Un hémogramme comprenant une numération lymphocytaire doit être réalisé à intervalles réguliers et de façon rapprochée en fonction du tableau clinique.
En cas de lymphopénie, une surveillance fréquente et étroite doit être menée afin de détecter tout signe ou symptôme de trouble neurologique.
Les patients doivent être informés du risque de LEMP et de l'importance de signaler rapidement des signes évocateurs : les premiers symptômes de LEMP peuvent être difficiles à différencier d'une poussée de sclérose en plaques (troubles cognitifs, psychiatriques ou visuels). Or le pronostic de la LEMP dépend de la précocité du diagnostic et de la rapidité de prise en charge.
En conséquence, si une LEMP est suspectée ou en cas de doute, le traitement par TECFIDERA doit être immédiatement interrompu.
Pour mémoire
TECFIDERA gélule gastrorésistante (120 mg et 240 mg) est indiqué dans le traitement des patients adultes atteints de sclérose en plaques de forme rémittente récurrente.
Ce médicament est commercialisé en France à l'hôpital depuis mars 2014 et pris en charge, en l'absence d'alternative thérapeutique, dans le cadre du relais d'ATU (avis du collège de la HAS publié le 23 juin 2014).
Sa prescription est réservée aux spécialistes en neurologie.
Pour aller plus loin
- Se reporter à la monographie VIDAL de TECFIDERA (mise à jour du 4 novembre 2014)
- Communiqué - Tecfidera (diméthyl fumarate) : un cas de leucoencéphalopathie multifocale progressive (LEMP) survenu chez un patient présentant une lymphopénie sévère et prolongée (ANSM, 8 décembre 2014)
- Lettre du laboratoire Biogen Idec aux neurologues, médecins généralistes et infirmières spécialisées dans la sclérose en plaques (sur le site de l'ANSM, décembre 2014)
- Meeting highlights from the Pharmacovigilance Risk Assessment Committee (PRAC) 3-6 November 2014
- Retour d'information sur le PRAC de novembre 2014 - Point d'Information de l'ANSM (14 novembre 2014)
- Synthèse d'avis de la Commission de la transparence (HAS, mai 2014)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.