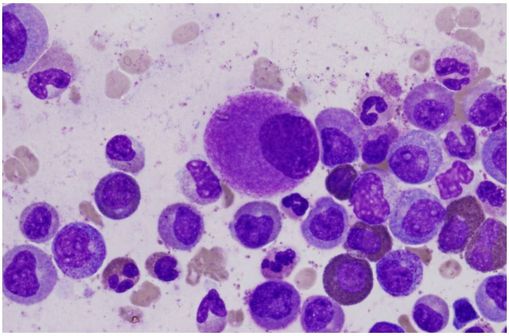
Mégacaryocyte de petite taille, hypolobé (au centre du cliché) sur une ponction de moelle, typique d'une leucémie myéloïde chronique (cliché @ Difu Wu sur Wikimedia anglais).
La réévaluation européenne de l'inhibiteur de la tyrosine kinase, ICLUSIG (ponatinib), est désormais finalisée : son rapport bénéfice risque est considéré positif par le Comité pour l'évaluation des risques en matière de pharmacovigilance (PRAC) de l'Agence européenne du médicament (EMA).
Une alerte donnée par la FDA fin 2013
Peu après sa mise à disposition en France dans les hôpitaux, ICLUSIG avait fait l'objet d'une alerte lancée fin 2013 par la Food and Drug Administration (FAD) : celle-ci avait observé une augmentation de la fréquence des événements thrombotiques artériels et veineux, dont certains d'évolution fatale tels des accidents vasculaires cérébraux, des infarctus massifs ou des ischémies périphériques.
Début décembre 2013, une lettre avait été adressée aux professionnels de santé français par le laboratoire ARIAD, en accord avec l'Agence de sécurité du médicament et des produits de santé, pour les informer des modifications apportées au résumé des caractéristiques du produit (RCP) visant à intensifier les mises en gardes sur le risque thrombogène artériel et veineux d'ICLUSIG.
RCP d'ICLUSIG : le PRAC recommande de nouvelles modifications
Bien que le PRAC considère que le rapport bénéfice/risque d'ICLUSIG reste positif, il émet plusieurs recommandations relatives à l'information sur son risque thrombogène :
- inclure dans le RCP des informations relatives à la dose dépendance du risque thrombogène d'ICLUSIG ; toutefois, une diminution de dose n'est pas formellement recommandée en l'absence de données disponible quant à l'efficacité de moindres doses ;
- chez les patients atteints de leucémie myéloïde chronique (LMC) ayant une réponse cytogénétique majeure mais présentant un risque d'évènement thrombotique, considérer une réduction de la dose d'ICLUSIG :
- en tenant compte notamment :
- des facteurs de risque cardiovasculaires du patient,
- du délais d'obtention de la réponse cytogénétique,
- du taux du transcrit BCR-ABL (breakpoint cluster region/Abelson),
- en surveillant étroitement la réponse cytogéntique ;
- en tenant compte notamment :
- arrêter le traitement par ICLUSIG en l'absence de réponse au traitement après 3 mois de traitement.
De nouvelles études à venir
Afin de répondre aux questions suscitées par cette réévaluation du rapport bénéfice/risque d'ICLUSIG, plusieurs études seront réalisées :
- une étude d'efficacité et de sécurité visant à évaluer, chez les patients en phase chronique de LMC, l'effet d'une diminution de la dose d'ICLUSIG sur le risque thrombogène et sur l'efficacité ;
- des études expérimentales pour préciser le mécanisme thrombogène du ponatinib.
Pour mémoire
ICLUSIG est indiqué chez les patients adultes atteints de :
- LMC en phase chronique, en phase accélérée ou en phase blastique, qui présentent une résistance au dasatinib ou au nilotinib ; une intolérance au dasatinib ou au nilotinib et pour qui un traitement ultérieur par imatinib n'est pas cliniquement approprié ; ou qui expriment la mutation T315I ;
- ou de leucémie aiguë lymphoblastique à chromosome Philadelphie (LAL Ph+), qui présentent une résistance au dasatinib ; une intolérance au dasatinib et pour qui un traitement ultérieur par imatinib n'est pas cliniquement approprié ; ou qui expriment la mutation T315I.
Pour aller plus loin
Meeting highlights from the Pharmacovigilance Risk Assessment Committee (PRAC) 6-9 October 2014, sur le site de l'EMA (10 octobre 2014)
Point d'information de l'ANSM : Iclusig (ponatinib), médicaments à base de testostérone, médicaments contenant du valproate et dérivés (divalproate de sodium / valpromide) - retour d'information sur le PRAC d'octobre 2014.
Sur VIDAL.fr
ICLUSIG comprimé pelliculé (ponatinib) : recommandations concernant les risques d'événements vasculaires occlusifs (6 Décembre 2013)
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute lâactualitÃĐ par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.