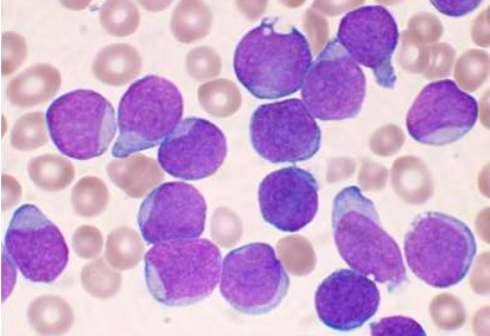
Cellules précurseurs de lymphocytes B d'une personne ayant une leucémie lymphoblastique aiguë (VashiDonsk, Wikimedia)
Suite à la mise à disposition d'ICLUSIG comprimé pelliculé sur le marché hospitalier français, le laboratoire Ariad Pharma France, en accord avec l'EMA (Agence européenne du médicament) et l'ANSM (Agence nationale de sécurité du médicament et des produits de santé), informe les professionnels de santé concernés d'un renforcement des mises en garde concernant le risque d'événements vasculaires occlusifs associé au ponatinib.
De nouvelles recommandations ont été émises afin de limiter la survenue de ces événements indésirables.
De nouvelles recommandations ont été émises afin de limiter la survenue de ces événements indésirables.
ICLUSIG, nouvel inhibiteur de la tyrosine kinase Bcr-Abl
ICLUSIG se compose de ponatinib, un nouveau principe actif de la classe pharmacothérapeutique des inhibiteurs de la tyrosine-kinase Bcr-Abl.
ICLUSIG comprimé pelliculé est indiqué chez les patients adultes atteints :
- de leucémie myéloïde chronique (LMC) en phase chronique, en phase accélérée ou en phase blastique, qui présentent une résistance au dasatinib ou au nilotinib ou une intolérance au dasatinib ou au nilotinib et pour qui un traitement ultérieur par imatinib n'est pas cliniquement approprié, ou qui expriment la mutation T315I ;
- ou de leucémie aiguë lymphoblastique à chromosome Philadelphie (LAL Ph+), qui présentent une résistance au dasatinib ou une intolérance au dasatinib et pour qui un traitement ultérieur par imatinib n'est pas cliniquement approprié, ou qui expriment la mutation T315I.
Deux dosages d'ICLUSIG comprimé pelliculé sont disponibles : 15 mg et 45 mg.
ICLUSIG est un médicament orphelin.
Ce médicament est sous surveillance renforcée. Sa mise à disposition s'est accompagnée de la mise en place d'un PGR (plan de gestion des risques) européen.
En France, ce médicament est commercialisé depuis le 1er octobre 2013. Auparavant, il était disponible sous le statut d'ATU (autorisation temporaire d'utilisation).
Evénements indésirables : les données disponibles
Une augmentation du nombre d'évènements thrombotiques artériels et veineux a été observée chez des patients traités par le ponatinib, lors du suivi prolongé de deux essais cliniques en cours, l'un de phase 1, l'autre de phase 2. Il s'agit d'évènements indésirables cardiovasculaires, cérébrovasculaires et vasculaires périphériques, ainsi que d'évènements thrombotiques veineux.
Ces événements sont apparus chez des patients avec ou sans facteurs de risque cardiovasculaire, y compris chez des patients âgés de 50 ans ou moins.
Les événements indésirables vasculaires occlusifs étaient plus fréquents chez les patients plus âgés et chez ceux présentant des antécédents d'ischémie, d'hypertension, de diabète ou d'hyperlipidémie.
Prescription : toujours possible mais avec précaution
La prescription d'ICLUSIG reste possible, à condition de respecter l'indication approuvée et de tenir compte des précautions suivantes :
- le ponatinib ne doit pas être prescrit chez les patients présentant des antécédents d'infarctus du myocarde ou d'accident vasculaire cérébral, à moins que le bénéfice attendu du traitement soit supérieur aux risques potentiels ;
- l'état cardiovasculaire des patients doit être évalué et les facteurs de risque cardiovasculaire doivent être pris en charge et contrôlés avant l'initiation du traitement par ponatinib. La surveillance cardiovasculaire doit se poursuivre tout au long du traitement par ponatinib ;
- l'hypertension artérielle doit être contrôlée au cours du traitement par le ponatinib. L'interruption du traitement par le ponatinib doit être envisagée en l'absence de contrôle de l'hypertension artérielle ;
- l'apparition de signes d'occlusion vasculaire ou de thromboembolie doit être surveillée ; en présence de tels signes, le traitement doit être interrompu immédiatement.
Le laboratoire souligne que le rapport bénéfice/risque doit toujours être évalué avant et pendant le traitement par ICLUSIG.
Sources et ressources complémentaires
- Communiqué - Iclusig (ponatinib) : nouvelles recommandations concernant les risques d'évènements vasculaires occlusifs (ANSM, 5 décembre 2013)
- Lettre du laboratoire Ariad aux onco-hématologues, hématologues, pharmaciens hospitaliers, investigateurs des essais cliniques utilisant le ponatinib (sur le site de l'ANSM, 2 décembre 2013)
- European Medicines Agency recommends changes in use of leukaemia medicine Iclusig (ponatinib) in order to minimise risk of blood clots, communiqué de presse de l'EMA (22 novembre 2013)
- Résumé des caractéristiques d'ICLUSIG, sur le site de l'EMA
- Résumé du rapport trimestriel N°1 et 2 - Autorisation Temporaire d'Utilisation Nominative - Ponatinib 15 mg, comprimé - Période du 23 août 2012 au 22 février 2013, sur le site de l'ANSM
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.